Поражение ногтей красным плоским лишаем
Красный плоский лишай ногтей
Проявления красного плоского лишая на ногтевой пластинке, ногтевом ложе и всей ногтевой фаланге разнообразны. Наиболее характерно чередование продольных желобков и гребешков на поверхности ногтя. В глубине желобков обнаруживают тонкие продольные трещины. Ногтевая пластинка истончается, дно канавок вследствие загрязнения приобретает темную окраску. Дистальный край ногтей часто расслаивается, мелкие частицы ногтя отпадают, образуя дефекты. У некоторых больных возникает одна медиально расположенная канавка, начинающаяся у свободного края ногтя и напоминающая каналеформную дистрофию. Изредка, наблюдаются поражения задних ногтевых валиков (покраснение, отечность, инфильтрация, пузырьки, эрозии, трещины). У одних больных исчезает ногтевая кожица, что часто наблюдается при кандидозе ногтевых валиков и ногтей, у других же при сильно выраженных воспалительных явлениях она срастается с остатками ногтевой пластинки в проксимальной ее части, образуя кожистый лоскут — птеригиум. У небольшой части больных красным плоским лишаем обнаруживают подногтевые папулы, имеющие красно-фиолетовый оттенок. При красном плоском лишае поражаются ногтевые пластинки пальцев кистей, реже стоп.
Дифференциальная диагностика. Поражение ногтей при красном плоском лишае следует отличать от псориаза, экземы, болезни Девержи, фолликулярного дискератоза Дарье, поражений, обусловленных грибами и бактериями. Если диагноз красного плоского лишая ногтей (редко ногтевых валиков) при наличии его проявлений на коже или слизистых оболочках установить сравнительно легко, то при изолированном их поражении диагностика затруднена. В пользу красного плоского лишая свидетельствуют следующие особенности клинической картины: продольная ребристость ногтя — сочетание гребешков с канавками, наличие продольных трещин, онихошизис (расщепление ногтевой пластинки со свободного края), уменьшение ногтевых пластинок в проксимально-дистальном направлении за счет потери вещества ногтя вследствие его расщепления и ломкости. В результате загрязнения канавок и трещин ноготь нередко приобретает темно-бурую, часто черную окраску. Степень выраженности дистрофических изменений находится в прямой зависимости от глубины поражения матрицы ногтя. У некоторых больных ногти поражаются по типу онихолизиса, когда ногтевая пластинка отторгается от ногтевого ложа начиная со свободного края, т. е. возникает анонихия. Может образоваться птеригиум ногтя. Важное значение в диагностике имеют результаты гистологических исследований ногтевого ложа пораженных ногтей при условии хорошего владения оператором техникой биопсии. В пользу красного плоского лишая свидетельствуют также гиперкератоз и гранулез ногтевого ложа, базально-клеточная дегенерация с непостоянным наличием меланина.
Ввиду некоторого сходства пораженных ногтей при красном плоском лишае и онихомикозах желательно провести микроскопическое и культуральное исследование. Изредка встречаются комбинированные поражения, когда дерматофиты и другая грибковая флора «наслаивается» на измененную основным процессом ногтевую пластинку.
Дата добавления: 2017-02-13 ; просмотров: 2494 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Красный плоский лишай: симптоматика, формы, лечение
Красный плоский лишай (lichen ruber planus, истинный лихен, лишай Уилсона) – хронический дерматоз, единственным внешним проявлением которого является наличие на теле папул, узелков красного цвета. Характеризуется повышенным зудом. Первые высыпания при красном плоском лишае держатся в течение нескольких недель или месяцев, рецидивы возникают на протяжении многих лет. Диагностируется заболевание достаточно просто, но требует длительного систематического лечения. Обращение к врачу при первых подозрениях на заболевание обязательно!

Возбудитель красного плоского лишая
Этиология данного заболевания до конца не изучена. Предполагается, что болезнь носит вирусный характер. Заболеть можно при сочетании нескольких факторов – нервного напряжения, неполноценного питания, генетической предрасположенности, аллергии, наличии инфекций и других.
Заразен или нет красный плоский лишай?
На этот вопрос не существует категорического ответа «да» или «нет». При длительном контакте с больным небольшой риск заразиться существует, однако только для людей с генетической предрасположенностью или слабым иммунитетом. Несмотря на это, стоит помнить о том, что красный плоский лишай довольно часто сочетается с хроническим вирусным гепатитом «C», возбудитель которого может передаваться от человека к человеку при определенных условиях.
Группа риска
Заболеть красным плоским лишаем можно в любом возрасте, однако больше всего диагнозов регистрируется у людей в возрасте от 30 до 60 лет. Причем женщины болеют им в 2 раза чаще, чем мужчины.
Факторы, способствующие возникновению красного плоского лишая
- Перенесенные стрессы;
- наследственная предрасположенность;
- заболевания желудочно-кишечного тракта;
- травмы слизистой оболочки рта;
- сахарный диабет;
- расстройства нервной системы;
- аллергические реакции;
- нарушения иммунитета;
- наличие очагов хронической инфекции в организме (кариес, тонзиллит, гайморит).
Симптомы красного плоского лишая
Для красного плоского лишая характерна сыпь, состоящая из плоских папул (узелков) красно-фиолетового или малиново-красного цвета диаметром 2-5 мм. Могут сливаться, при этом образуются бляшки, вокруг которых появляются новые папулы, имеющие втянутую середину и блестящую поверхность. Шелушение незначительно, чешуйки трудно отделяемые.
Высыпания при красном плоском лишае множественные, располагаются группами в виде гирлянд, колец или линий. После излечения заболевания кожа на участках поражения долгое время остается гиперпигментированной.
Сопровождается заболевание сильным зудом.
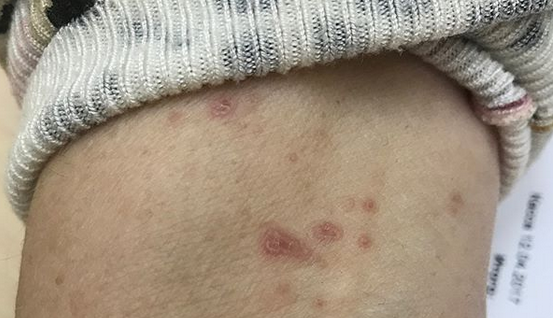
Локализация красного плоского лишая
Чаще всего этот вид лишая поражает кожу сгибательной поверхности конечностей, внутренней поверхности бедер, подмышечных и паховых областей, туловища, слизистую оболочку полости рта. Также может наблюдаться поражение ногтей: продольные полосы, гребешки, помутнение ногтевой пластинки, разрушение ногтевого валика.
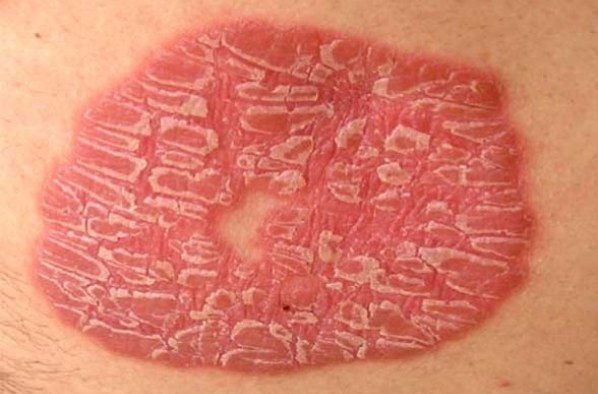
Ладони, подошвы, волосистая часть головы и лицо обычно не подвержены поражению красным плоским лишаем, хотя такие случаи изредка регистрируются.
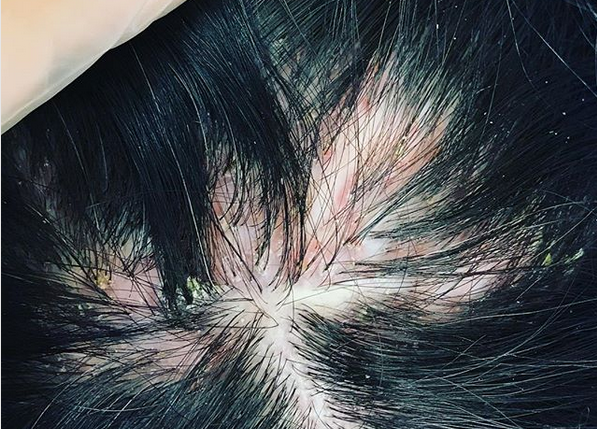
Поражение слизистой оболочки половых органов и рта наблюдается почти у 50 % больных. Причем примерно у четверти оно не сопровождается высыпаниями на коже.
Поражение ногтей отмечается в 10–15 %.

Классификация по времени течения
По течению красный плоский лишай бывает:
- острым – продолжается до одного месяца;
- подострым – до шести месяцев;
- длительно протекающим – более шести месяцев.
Стадии заболевания
Как хроническое заболевание красный плоский лишай протекает с периодами ремиссии и рецидивов, которые могут повторяться от 1 до 5 раз в течение года, даже несмотря на лечение.
В клиническом течении заболевания различают такие стадии:
- острая, или подострая;
- прогрессирующая (на фоне имеющихся и увеличивающихся в размерах папул появляются новые высыпания или эрозии и язвы, отек, покраснение – в зависимости от формы заболевания, сопровождающиеся интенсивным зудом);
- стационарная (прекращение прогрессирования);
- стадия разрешения (иногда с образованием пятен избыточной пигментации);
- ремиссия (затухание).
Типичная и атипичные формы красного плоского лишая
Разнообразие внешнего вида папул, их локализации и группировки обуславливает большое количество клинических форм красного плоского лишая. В официальной медицине различают 7 форм:
- типичная;
- кольцевидная;
- эритематозная;
- веррукозная;
- пемфигоидная;
- атрофическая;
- язвенная.
Типичная форма проявляется в виде мелких серых папул, по мере развития болезни на коже образуются бляшки с блестящей поверхностью. Такие же высыпания на слизистой оболочке имеют матовый цвет, со временем они могут преобразоваться в язвочки.
Кольцевидная – локализуется в области наружных половых органов в виде кольца, отсюда ее название. Именно это служит первым симптомом красного плоского лишая.
Эритематозная – отличается от предыдущих форм мягкими на ощупь папулами малинового или ярко-розового цвета.
Бородавчатая – проявляется плоскими папулами со вдавленной серединой на коже и слизистой рта и сильным зудом. Края папул покрыты чешуйками.
Пемфигоидная форма отличается от предыдущей тем, что на месте папул образуются пузырьки с жидкостью, которые со временем лопаются (впоследствии на их месте может остаться гиперпигментация).
Атрофическая сопровождается дополнительным образованием на коже белых пятен с перламутровыми островками.
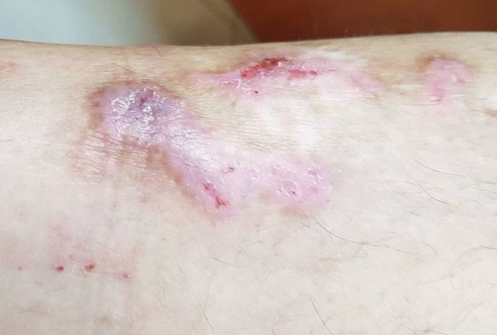
Язвенная форма предполагает образование язв, иногда с белым налётом. Как правило, после излечения на месте таких поражений остаются округлые шрамы.
В целом, атипичных форм красного плоского лишая существует более 15. Кроме рассмотренных выше, регистрируются:
- веррукозная форма;
- буллезная, или пузырная;
- фолликулярная;
- эрозивно-язвенная;
- пигментная и другие.

Диагностика красного плоского лишая
Для установления диагноза необходимо обратиться к дерматологу. Для того, чтобы уточнить диагноз и исключить другие заболевания, схожие по симптоматике, врач может назначить дополнительные исследования.
Дифференциальная диагностика красного плоского лишая проводится с такими болезнями:
- лейкоплакия;
- кандидоз;
- красная волчанка;
- папулезный сифилис;
- аллергический стоматит;
- хроническая травма;
- болезнь Боуэна.
При лейкоплакии в отличие от красного плоского лишая пораженный участок слегка возвышается над уровнем слизистой и имеет вид сплошной белесоватой бляшки, вокруг которой слизистая оболочка не изменена. Папулы отсутствуют. В отличие от красного плоского лишая участки поражения локализуются преимущественно в передних отделах полости рта – на слизистой углов рта и щек.
При кандидозе на слизистой оболочке рта нет четкого рисунка. При соскабливании белый налет снимается частично или полностью (папулы при лишае не удаляются).
При красной волчанке папулы расположены в основном на губах, щеках, реже – на небе. Папулы по периферии очага поражения отсутствуют.
Папулы при сифилисе отличаются от красного плоского лишая большими размерами, имеют круглую или овальную форму. Их поверхность покрыта серовато-белым налетом, легко снимающимся при соскабливании.
Отличить аллергический стоматит от красного плоского лишая можно на основе анализа данных анамнеза пациента, а также результатов аллергологических проб.
В целом, сложности с установлением диагноза возникают лишь при атипичных формах болезни.
Лечение красного плоского лишая
Для лечения красного плоского лишая обычно прописываются препараты такого спектра:
- успокаивающие средства;
- антидепрессанты;
- гормональные препараты;
- антиаллергические препараты.
Мази при таком заболевании обязательны, как и при других формах грибковых заболеваний – не только для уменьшения симптоматики, но и для отшелушивания ороговевших клеток.
Поскольку при красном плоском лишае значительно страдает иммунитет, больному могут прописать курс витаминов внутривенно.
При хроническом течении недуга в программу лечения обязательно включают препараты, улучшающие кислородное обеспечение тканей организма.

Диета при красном плоском лишае
Диета при этом виде заболевания обязательна. Во время лечения из рациона следует исключить алкоголь, копчености, жирное мясо, кофе, яйца, соки, газированные напитки, острые приправы, сладости с красителями.
Курение также под запретом.

ВАЖНО! Использовать любые лекарственные средства самостоятельно, без точной постановки диагноза и консультации врача, при такой форме лишая крайне опасно!
Мнение редакции может не совпадать с мнением автора статьи.
Автореферат и диссертация по медицине (14.00.11) на тему: Красный плоский лишай (современные иммунологические и биохимические аспекты) и методы патогенетической терапии

Автореферат диссертации по медицине на тему Красный плоский лишай (современные иммунологические и биохимические аспекты) и методы патогенетической терапии
) 1 Министерство здравоохранения
и медицинской промышленности РФ
с,ЦЕНТРАЛЬНЫЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ КОЖНО-ВЕНЕРОЛОГИЧЕСКИИ ИНСТИТУТ
СЛЕСАРЕНКО Наталия Александровна
КРАСНЫЙ ПЛОСКИЙ ЛИШАЙ
(современные иммунологические и биохимические аспекты)
МЕТОДЫ ПАТОГЕНЕТИЧЕСКОЙ ТЕРАПИИ
14.00.11 — кожные и венерические болезни
Автореферат диссертации на соискание учёной степени доктора медицинских наук
Работа выполнена в Саратовском государственном медицинском университете
Научный консультант: доктор медицинских наук профессор С. И. Довжанский.
доктор мед. наук профессор Антоньев А. А. доктор мед. паук профессор Вербенко Е. В., доктор мед. наук профессор Петрова И. В.
Ведущее учреждение: Санкт-Петербургская Военно-медицинская академия.
Защиту состоится г.
в . часов на заседании Специализированного совета (Д-074.10.01) при Центральном научно-исследовательском кожно-венерологпческом институте Министерства здравоохранения и медицинской промышленности Российской Федерации (107076. Москва, ул. Короленко, д. 3).
С диссертацией можно ознакомиться в библиотеке института.
Автореферат разослан 1995 г.
Ученый секретарь Специализированного совета кандидат медицинских наук
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы.Красный плоский лишай (КПЛ)^ один из распространенных дерматозов. В общей структуре дерматологической заболеваемости он составляет 0,16 — 1,2% и до 35% — среди болезней слизистой оболочки рта (Маш-киллейсон А. Л., 1984, Nasemann, Sauerbrey, 1974, Hollander, 1979; Kleine — Natrop, 1984). Эрозивно-язвенные формы КПЛ рассматриваются как преканцерозы. Число больных этим дерматозом неуклонно растет. Чаще стали болеть дети. Мучительный зуд, обилие высыпаний, разнообразие клинических форм и.вариантов течения КПЛ нередко вызывают длительную потерю трудоспособности больных, неустойчивость их пспхо-эмоционалыюй сферы (Аптоньев А. А. и соавт., 1982).
Красный плоский лишай отличается от многих других кожных заболеваний частотой сочетания с различными соматическими болезнями, кроме того, описываются лихеноидные поражения пищевода, желудка, кишечника, мочевого пузыря, матки, что позволяет говорить о системности патологического процесса (Потекаев Н. С. и соавт., 1964, Машкиллейсон А. Л. и соавт., 1980, Шинскнй Г. Э., Чучалина О. М., 1982, Довжан-ский С. И. и соавт., 1985, Grinspan и соавт., 1966, Sollberg, 1980, Fellner, 1980, Horn —Stein, 1984, Patrone и соавт., 1986, Silverman и соавт., 1991, Elluj и соавт., 1992, Holder и соавт., 1992).
В связи с современными представлениями о коже как органе иммунной системы и появлением лихеноидных высыпаний при различных аутоиммунных, онкологических заболеваниях, реакции отторжения трансплантата (graft versus host Disease — qVhD), возникающей после пересадки органов и тканей, КПЛ привлекает к себе внимание не только дерматологов и стоматологов, но и терапевтов, хирургов, онкологов, иммунологов, трансплантологов.
В настоящее время, в связи с обострением экологических проблем и возрастанием антигенной нагрузки на организм человека, приводящей не только к функциональным, но и структурным нарушенням гомеостаза, роль кожи в защит-
ных механизмах весьма существенна. Иммунопатологические процессы в ней сложны и многообразны. Патоморфологиче-ская картина КПЛ с характерной для нее лимфоцитарной инфильтрацией дермы, проникновением иммунокомпетентных клеток в эпидермис, дистрофией и разрушением кератиноци-тов вплоть до некроза, апоптоза и образования «пустот» и одновременным включением процессов регенерации, представляет тканевую реакцию гиперчувствительности замедленного типа (ГЗТ) (Каламкарян А. А. и соавт., 1990, Goos, 1978, Röcken, 1988, Gianotti, Panfilis, 1989, Abraham, Feuerman, 1992). Несмотря на это свидетельство включения иммунных механизмов, сложность взаимоотношений патологического процесса и нормальных защитных реакций, и возросший интерес к этому заболеванию, сведения о состоянии иммунитета у больных КПЛ немногочисленны и противоречивы (Чахки-ев Р. О., 1980, Розыева А. А., 1981, Абудуев Н. К-, 1989, Трофимова И. Б. и соавт., 1990).
Мало работ по оценке иммунного статуса больных КПЛ на основе комплексного патогенетически обоснованного, двух-и трехуровневого подхода к функционированию иммунной системы, учитывающего процессы распознавания, активации, пролиферации, трансформации иммунокомпетентных клеток, влияния медиаторов и генетических «маркёров».
Несмотря на роль лекарственных и химических веществ в развитии КПЛ, отмечаемую многими авторами, не исследовались процессы микросомального окисления и апеллирования, ответственные за биотрансформацшо и элиминацию ксенобиотиков и собственных токсических метаболитов, другие окислительно-восстановительные и нейро-гуморальные реакции, имеющие определенное значение-в развитии дистрофических явлений в коже и слизистой, столь характерных для данного заболевания.
Клинические варианты КПЛ многочисленны, сообщения о них, в основном, имеют описательный характер. Нет четкой классификации, объединяющей эти формы на основе общего механизма развития.
Лечебно-тактические вопросы ведения больных этим заболеванием всегда представляют достаточные трудности. Предлагаемые методы лечения большей частью имеют целью воздействие на один из механизмов развития дерматоза, тем более, они не учитывают фазу патологического процесса, взаимодействия защитных и регенеративных реакций, роль провоцирующих факторов экзо- или эндогенного характера.
Цель и задачи исследования.
Целью работы является уточнение механизмов развития красного плоского лишая как лихеноидной реакции кожи и слизистой, дифференциальная диагностика вариантов этой реакции и определение ее места в общей патологии человека в аспектах иммунных и метаболических процессов организма, а также возможности регуляции с учетом защитной и патогенной роли.
Для достижения цели были поставлены задачи:
1. Изучить многочисленные формы и варианты течения КПЛ и систематизировать их с учетом клинической картины и провоцирующих факторов.
2. Оценить характер взаимосвязи иммунного статуса больных КПЛ, исследуемого на основе современного двух- и трехуровневого патогенетического подхода к функционированию иммунокомпетентных клеток, учитывающего процессы их активации, пролиферации и дифференцировкп, с клиническими проявлениями заболевания, его фазой и степенью вовлеченности эпидермально-дермальных структур.
3. Изучить состояние иммунокомпетентных клеток (в частности, лимфоцитов) в очаге поражения с помощью электронной микроскопии и сопоставить его с результатами исследования их функциональной активности в кровяном русле.
4. Исследовать процессы микросомалыюго окисления и ацетилирования, ответственных за детоксикацию и выведение различных ксенобиотиков и собственных токсичных метаболитов, возможно, играющих определенную роль в стимуляции лихеноидных реакций.
5. Исследовать процессы кислородного обеспечения тканей, окислительно-восстановительные реакции в системе пере-кисного окисления липидов (ПОЛ), некоторые нейро-гумо-ральные регуляции, которые могут, в какой-то степени, участвовать в воспалительных и дистрофических изменениях, характерных для патоморфологии КПЛ.
6. Разработать тактику ведения и методы дифференцированного патогенетически обоснованного, этапного лечения, направленного на восстановление гомеостаза у больных с лихе-ноидными реакциями.
Научная новизна работы заключается в том, что она раскрывает новые механизмы развития красного плоского лишая, позволяет определить место заболевания в общей патологии
человека как интенсивной иммунной клеточной реакции —■ гиперчувствительности замедленного типа (ГЗТ) в ситуации «хозяин против хозяина» (РХПХ), с учетом ее защитной и патологической роли, этапов развития и вовлеченности эпи-дермально-дермальных структур, и тем самым открывает перспективу дальнейшего изучения дерматоза в аспекте понимания роли кожи в поддержании иммунного гомеостаза.
Проведенные исследования позволяют трактовать различные формы КПЛ степенью вовлеченности в патологический .процесс иммунных, воспалительных, дистрофических и регенеративных механизмов ГЗТ и объяснить признаки появления поражения соединительной ткани и сочетание с аутоиммунными заболеваниями ослаблением защитной роли этой реакции и включением других иммунных нарушений.
В работе впервые, на основании фактического материала, показана этиотропная полиморфность лихеноидных реакций кожи и слизистой, традиционно трактующихся как атипичные формы КПЛ.
Предложены новые методы дифференцированного лечения, основанные на учете провоцирующих факторов и этапности механизмов развития заболевания во всем его многообразии.
Практическая значимость работы.
1. Предложена интегральная концепция развития красного плоского лишая как своеобразной лихеноидной реакции, позволяющая объединить многочисленные формы и варианты течения дерматоза и учесть провоцирующие факторы.
Дифференциально-диагностические критерии (диагностический алгоритм) разграничения лихеноидных реакций позволяют врачу даже в амбулаторных условиях выбрать тактику ведения и лечения больного.
2. Дана общая оценка иммунного статуса больных КПЛ, свидетельствующая о преобладании клеточных реакций в иммунном ответе, его незавершенности, состоянии экзо- и эндогенной стимуляции, зависимости от фазы патологического процесса.
3. Исследования метаболических процессов, в частности микросомального окисления и ацетилирования, ответственных за дезинтоксикационную функцию организма, а также окислительно-восстановительных реакций в системе ПОЛ и АОС, кислородного обеспечения тканей, показали возможную роль
их нарушений в заболевании. В результате в плане ведения больного предложены методы коррекции этих изменений.
4. Проведено изучение in vitro влияния отечественного иммуномодулятора вилозена на функциональную активность лимфоцитов больных КПЛ, показана его нормализующая роль в иммунном ответе. Впервые он предложен с этой целью для лечения больных КПЛ.
5. Разработаны методы комплексного дифференцированного, патогенетического, этапного лечения больных КПЛ. Проведено сравнение результатов коррекции иммунных нарушений несколькими препаратами (вилозен, кортикостероиды, пресоцил, фторафур). Предложен план лечения, где обозначена цель лечебного воздействия и используемые препараты.
Внедрение в практику.
По материалам исследования составлены учебно-методи-ческне рекомендации «Диагностика и лечение красного плоского лишая у взрослых и детей», утвержденные Ученым советом педиатрического факультета Саратовского государственного медицинского университета (протокол № 6 от 11 июня 1991 года).
Методические рекомендации используются в практической работе и в обучении студентов и врачей Саратовского, Одесского, Ижевского, Уральского мединститутов, Казанского ГИДУва, лечебно-профилактических учреждений России, Украины, Удмуртии, Татарстана, о чем имеются акты внедрения.
Имеется авторское свидетельство на- изобретение № 1803115 «Средство для лечения красного плоского лишая», зарегистрированное в Государственном реестре изобретений СССР от 9 октября 1992 года, н рационализаторское предложение «Вилозен в лечении больных красным плоским лишаем» № 1876, 1991 год.
Материалы диссертации доложены и обсуждены на 2-м Международном симпозиуме «Реабилитация иммунной системы» (Кутаиси — Цхалтубо — Сочи «Дагомыс») в 1990 году, иа юбилейной конференции, посвященной памяти В. А. Рахманова, в Московской медицинской академии им. И. М. Сеченова 5 февраля 1993 г., на заседаниях Саратовского филиала Всероссийского научного медицинского общества дермато-венерологов в 1992 и 1993 годах.
На IX Всесоюзном съезде дермато-венерологов, проводимом в сентябре 1991 года в Алма-Ате, по материалам диссертации представлен, стендовый доклад «Функциональная активность лимфоцитов у больных красным плоским лишаем», включенный в программу съезда.
По материалам диссертации опубликовано 28 научных работ, 26 из них — в центральной печати, издана монография «Красный плоский лишай» в соавторстве с С. И. Довжан-ским.
Положения, выносимые на защиту.
1. В основе развития различных форм красного плоского лишая лежит лихеноидно-тканевая реакция, формирующаяся, главным образом, как этапы гиперчувствительностп замедленного типа с присущими ей’иммунными, воспалительными, дистрофическими и регенеративными механизмами в аспекте ее защитной и патологической роли.
Факторы, провоцирующие лихеноидные реакции, многообразны, они могут быть экзо- или эндогенного характера и определяют клиническую картину заболевания, его течение и прогноз.
2. Современная оценка иммунного статуса больных КПЛ показывает активацию Т-клеточного звена иммунного ответа, его незавершенность и участие этих нарушений в патогенезе заболевания.
3. Интенсивная клеточная иммунная реакция у больных КПЛ направлена против собственных (аллогенных) структур. Доказательством существования ситуации «хозяин против хозяина» (РХПХ) служит циркуляция в кровяном русле больных КПЛ большого количества (в 2 раза превышающее нормальные показатели) делящихся, малодифференцированных лимфоцитов, определяемых как ДНК-синтезирующие, а также активация ядерного хроматина, кодирующего генную транскрипцию клеток, наиболее устойчивую к воздействиям любых митогенов, определяемые на всех’этапах развития патологического процесса, что свидетельствует о постоянной стимуляции иммунокомпетентных клеток, столь характерной для реакции отторжения трансплантата.
Электронно-микроскопическая картина лимфоцитов в очаге поражения соответствует, основному морфологическому
выражению ГЗТ и свидетельствует об их агрессии’ против собственных эпидермальных структур.
4. Метаболические изменения окислительно-восстановительных реакций в системе микросомалыюго окисления и ацетилирования, перекнсного окисления липидов (ПОЛ), кислородного обеспечения тканей играют -определенную роль в эндогенной стимуляции иммунных нарушений, определяя, в основном, хроническое течение заболевания.
5. Тактика ведения больных КПЛ не может ограничиваться констатацией имеющихся высыпаний. С помощью предложенного диагностического алгоритма выясняется характер провоцирующего лихеноидную реакцию фактора, определяется фаза патологического процесса. С учетом этого назначается дальнейшее обследование или дифференцированные методы коррекции иммунного ответа и метаболических нарушений.
Отечественный иммуномодулятор «Вилозен» наиболее эффективен при острой фазе заболевания в группе больных с экзогенной его стимуляцией.
Кортнкостероидные препараты назначаются больным тяжелыми формами КПЛ (экзантемные, буллезные элементы, явления общей интоксикации) совместно с ингибитором системы цнтохрома Р-450 а-токоферолом, что позволяет уменьшить дозу глюкокортикоида и сократить сроки лечения.
Коррекция выявленных метаболических нарушении у больных с хроническим торпидным или рецидивирующим течением лихеноидных реакций необходима, так как она позволяет нормализовать иммунные реакции и добиться стойкой ремиссии или выздоровления.
Структура и объем работы.
Диссертация состоит из введения, обзора литературы (глава 1), описания материала и методов исследования (глава 2), трех глав собственных исследований (глава 3 — «Клиника», глава 4 — «Иммунологические и биохимические исследования», глава 5 —■ «Лечение»), заключения, выводов, приложений и списка использованной литературы, включающего 202 отечественных и 266 иностранных работ. Диссертация иллюстрирована 36 таблицами и 43 рисунками, из которых 8 фотографий,
1. Материалы и методы исследования.
Работа выполнена на материале клинического наблюдения и обследования 325 больных красным плоским лишаем. Для контроля обследовалось 100 здоровых лиц (матери больных детей детского отделения и доноры).
Были проведены клинические исследования в динамике течения болезни, в процессе лечения и после него. Отдаленные результаты лечения оценивались спустя шесть месяцев — два года.
Были изучены: цельная кровь, сыворотка, выделенные из крови иммунокомпетентные клетки, биопсийный материал кожи больных и моча.
Больные были распределены на группы в зависимости от фазы патологического процесса (острая и хроническая), отмечалось течение заболевания (острое, подострое, хроническое) и его стадии (прогрессирование, стабилизация и регресс). Кроме критериев по клинической картине обследуемые группы образовывались по факторам «риска» (предполагаемым аспектам этиологии или параэтиологическим моментам):
1-я группа — больные, провоцирующим фактором хмаиифе-стации КПЛ у которых был инфекционный стимул (вирус?);
2-я группа —’ провоцирующий фактор — стимулирующая нагрузка экзогенного характера; 3-я группа — стимулирующая нагрузка эндогенного характера.
• В работе использовались клинические наблюдения, иммунологические, биохимические, физико-химические (препаративные электрофоретические, хемилюминесцентные, радиоизотопные) и электронно-микроскопические исследования.
Иммунологические исследования были выбраны основываясь на современных методах, учитывающих количественные и функциональные характеристики иммунокомпетентных клеток, медиаторов иммунной системы, генетических «маркёров». Исследовались процессы активации, пролиферации и трансформации иммунокомпетентных клеток.
Кровь у людей получали из локтевой вены или из пальца. В качестве антнкоагулянта использовали гепарин. Лимфоциты выделяли путем центрифугирования в градиенте плотности фиколл-верографин (с1= 1,077 г/см3). Затем готовили клеточную взвесь (3,0- 10е кл/мл) в среде 199 (3 части) и реактиве Хенкса (1 часть) (Воуйт, 1968).
В качестве неспецифических антигенов стимуляторов использовали фитогемагглютиннн (ФГА), конканавалин А. (КоА) и знмозан.
В-лимфоциты в крови определялись методом, основанным на идентификации клеток, имеющих рецептор к С3-ком-поненту комплемента и образующих розетки (ЕАС— РОК) с эритроцитами, нагруженными комплексом антитело — комплемент, а также по выявлению поверхностных иммуноглобулинов (A, G, М) в реакции иммунофлюоресценции с помощью антиглобулпновых сывороток, меченных флюорохро-мом (Новиков Д. К., Новикова В. И., 1979, Никитин В. М., 1982, Петров Р. В., 1987). Использовались сыворотки производства ЫИИЭМ им. Н. Ф. Гамалеи.
Т-л и м ф о ц и т ы исследовались методом, основанным на принципе спонтанного розеткообразования (Е — РОК) с эритроцитами барана (Петров Р. В. и соавт., 1982, Белокриниц-кнй Д. В., 1987), а также с использованием моноклональных антител против СД8 и СД4-рецепторов (йегер Л., 1990).
Содержание иммуноглобулинов основных классов (A, G, М) определяли общепринятым методом «по Мапчиии» (Mancini и соавт., 1965).
Определение циркулирующих иммунных комплексов (ЦИК) в сыворотке крови проводилось путем их осаждения полиэтиленглнколем — 6000 (ПЭГ-6000) в модификации, предложенной В. Е. Логинским и соавт. (1983).
Активация лимфоцитов песпецифическим митоге-‘ ио»м — ФГА, их реакция бласттрапсформации (РБТЛ) регистрировалась методом хемнлгоминесценцни (ХЛ) (Meretey и соавт., 1983) на ¡приборе ХЛМГЦ-01 в течение 10 мин. Уровень ее выражался индексом стимуляции (ИС), представляющим отношение исходной ХЛ (до внесения ФГА) к ХЛ на максимуме реакции. Кроме того, для оценки РБТЛ использовали радиологический метод включения ЗН-тимндина, с помощью которого определяли и содержание интерленкииов — ИЛ-1 и ИЛ-2. Метод основан на способности стимулированных ми-тогеном лимфоцитов увеличивать синтез ДНК, сопровождающийся включением в нее меченного тритием тнмпдина (Шютт X., 1987). Был применен ЗН-тнмидин фирмы Ашег-sham (США) с удельной активностью 17MeBg/mM. Количество изотопа, вносимое в одну пробу, составляло 37GBg в 5 мкл. Подсчет радиоактивности исследуемых проб проводили на бета-спектрометре для счета бета-излучения жидким сцинтиляционным методом Mark II (Германия).
Для оценки активности ЙЛ-1 использовали метод, основанный на его способности вызывать комнтогенный эффект у тимоцигов мышей линии СБА в присутствии субоптимальных концентраций неспецифических митогенов (Oppenheim и соавт., 1986).
Активность ИЛ-2 тестировали по способности данного лнмфокина поддерживать рост î-клеток, активированных ми-тогеном КоА. Активированные КоА-бласты получали из спле-ноцитов мышей линии СВА, в качестве контроля использовали стандартный препарат ИЛ-2 (Меримская О. С. и соавт., 1986, Gillls, Smith, 1977).
Определение концентрации АТФ в лимфоцитах проводилось методом люминолзависнмой ХЛ с использованием системы люциферин — люцифераза (Meretey и соавт., 1983).
Элекгрофоретическую подвижность (ЭФП) лимфоцитов исследовали методом непрерывного свободного распределительного электрофореза на аппарате Elphor Vap-5 фирмы Bender Hobein (ФРГ).
Регистрация соотношения лимфоцитов, находящихся в различных фазах клеточного цикла по содержанию в них ДНК, проводилась с использованием проточного цитофлюорн-метра 1СР22 фирмы «PHYWE» (Barlogie и соавт., 1976). Расчет клеток, находящихся отдельно в каждой фазе клеточного цикла, проводили с помощью математической модели, предложенной Baisch и соавт. (1975).
Методом проточной цитофлюориметрии на том же импульсном проточном цигофлюоримегре- 1СР22, сопряженном с IBM-совместимым компьютером, используя флюорохром акридиновый оранжевый (АО), исследовали состояние хроматина ядер и лизосомального аппарата иммуно-компетентных клеток, которые представляли трехмерными гистограммами (Melamed и соавт., 1974).
Антигены главного комплекса гистосовместимости — HLA-фенотип устанавливали в стандартном микролимфоцито-токсическом тесте с использованием набора сывороток Санкт-Петербургского НИИ гематологии и переливания крови и коммерческих HLA-сывороток фирмы Beheing. Использовали методику Tereseki и соавт. (1978) в модификации В. Ф. Со-хина и Е. Д. Чернушенко (1984). Относительный риск заболевания рассчитывали по формуле Woolf (1955), атрибутивный — по формуле:
где d и Р — частота антигенов среди больных и здоровых ¿6-
Ультратонкие срезы бпопеяйного материала кожи (больные КПЛ и здоровые лица), подготовленного по общепринятым методикам и заключенного ft смолу эпон-аралдит, подвергнутую в дальнейшем полимеризации, контрастировали уранил-ацетатом и цитратом свинца,’ просматривали и фотографировали в электронном микроскопе IEM-100-S (Япония).
Характеристику кислотно-щелочного и газового состава (КЩ ГС) артериальной и венозной крови проводили на аппарате «микро-Аструп» (Дания). С пом’ощыо полученных результатов и используя общепринятые математические формулы (формула Эпиингера и артерио-венозное различие по кислороду), судили о кислородном обеспечении крови и тканей больных КПЛ.
Для оценки процессов м и к р о с о м а л ьн ого окисления (детоксицнрующей функции печеночных оксигеназ в системе цитохрома Р-450) использовали метод определения полуэлиминации антипирина (Геллер Л. И. и соавт., 1982).
А ц е т и л и р о в а н и е изучалось по конституционному маркеру-ферменту N-ацетилтрансферазе методом С. Пребстин-га и И. П. Гаврилова в модификации Н. А. Тимофеевой (1971). В основе метода лежит получение окрашенного соединения в результате сочетания диазотпрованного сульфаниламида с ацетнлированной Н-кнслоТой.
Для оценки состояния перекисного окисления липидов (ПОЛ) определяли ацетнлгидроперекпеи — АГПЛ (метод Л. А. Романовой и И. Д. Стальной, 1977), суммарную пероксидазную активность — СПА (спектрофотометри-ческий метод Г. Н. Попова, Л. А. Нейковской, 1971, Ishihara, 1978), малоновый диальдегид — МДА) (с помощьютиобарби-туровой кислоты по методике И. Д. Стальной и Т. Г. Гариа-швилп, 1977, в модификации Т. Н. Федоровой и соавт., 1983).
О состоянии антиокендантной системы (ДОС) судили по определению ее ключевого фермента — супероксиддисмута-зы-СОД (метод Tried, 1975, методика Е. Е. Дубининой и соавт., 1983) и церулоплазмина (фотометрический метод Рэвина в модификации Ф. И. Комарова и соавт., 1981).
Кроме того, для одновременной оценки интенсивности сво-боднорадикальных окислительных процессов и активности
бнооксидантных систем организма исследовали хемилюмине-сценцию (ХЛ) цельной крови больных КПЛ и здоровых лиц (Стукова Н. Ю., 1991).
2. РЕЗУЛЬТАТЫ РАБОТЫ И ИХ ОБСУЖДЕНИЕ
2.1. Клинические наблюдения.
Наблюдая в течение 10 лет 325 больных в возрасте от 4-х до 82 лет с различными формами и вариантами КПЛ, мы систематизировали их с учетом клинической картины и провоцирующих факторов.
По течению КПЛ подразделяли на: 1) острый или под-острый с последующим выздоровлением и 2) хронический (длительно протекающий без ремиссий или рецидивирующий).
При диагностике учитывали характер первичного элемента, их локализацию, расположение относительно друг друга.
Рассматривая КПЛ как лихеноидно-тканевую реакцию кожи и слизистой и учитывая основную роль ГЗТ в ее формировании с иммунными, воспалительными, дистрофическими и регенеративными механизмами, присущими этой реакции, многочисленные формы дерматоза, определяемые по характеру морфологического элемента, трактовали как фазы (этапы) развития единого патологического процесса. В связи с этим выделяли две фазы заболевания — острую (воспалительные, дистрофические механизмы ГЗТ) и хроническую (пролифера-тивные и регенеративные ее этапы). При острой фазе клинически наблюдались экзантемные, папулёзные, буллёзные элементы, при хронической — гипертрофические, атрофиче-ские, пигментные. Кроме того, при хронической фазе имелись признаки поражения соединительной ткани (фиброз, склероз, атрофия, понкилодермия) у 28 больных (9,5%). У 26 больных (8,6%) высыпания КПЛ сочетались с клиническими проявлениями диффузных болезней соединительной ткани (склеродермия, дискоидная красная волчанка), аллергических вас-кулитов, буллёзного пемфигоида. Эти факты позволили говорить о лихеноидных реакциях кожи в рамках красного плоского лишая и близких по механизму развития заболеваний.
Анализируя истории развития КПЛ у 325 больных и учитывая возможную роль в манифестации высыпаний провоцирующих факторов, которые мы подразделяли на ангропо- и
экогенные (экзо- и эндогенного происхождения), из многообразия предполагаемых примни болезни в аспекте этнологии (даже если они являются параэтнологическими), мы выделили три основные: 1) инфекционный стимул (вирус?), 2) стимуляторы экзогенного характера (лекарственные, химические вещества бытового, профессионального и экологического происхождения), 3) стимуляторы эндогенного характера (собственные метаболиты, трансформированные лекарственные вещества и другие ксенобиотики, лпганды). Соответственно характеру провоцирующих факторов было образовано три группы больных (1, 2, 3).
Каждая из предполагаемых причин обусловливает не только клиническую картину морфологических элементов, но и характер течения заболевания, его прогноз, контингент больных. Напротив, клиническая картина помогает выяснить и учесть фактор развязывания болезни.
1-я группа—116 больных (35,6%). Высыпания КПЛ возникли на фоне переохлаждения, катаральных явлений, ОРВИ, гриппа, ангины. Больные отличались преимущественно молодым возрастом (от 4 до 42 лет), отсутствием хронических соматических заболеваний. Клиническая картина — типичные папулы, очень обильные, расположенные п типичных местах. Нередко в крупных складках они приобретают вытянутую форму «медальона». Поражение слизистой характерно (17,5%). На слизистых — папулы опалового цвета. Зуд характерен, но быстро исчезает. После разрешения — пятна бурого или коричневого цвета. Течение острое или подострое. Рецидивов, как правило, нет.
2-я группа — 52 больных (19,9%).В клинической картине помимо типичных узелков присутствуют экзангемные, буллёз-ные элементы. Поражается весь кожный покров или открытые участки. Высыпания на слизистой не характерны. Рецидивы редки.
3-я группа— 157 больных (54,2%). Помимо типичных узелков часто наблюдаются гипертрофические очаги и бляшки, очень характерна пигментация (пигментные пятна, венчик коричневого цвета вокруг типичных узелков, гипертрофических бляшек), атрофия, возникающая как бы первично, но тоже с венчиком гиперпигментации. Элементы крупные, часто сливаются в бляшки и очаги. Поражается слизистая рта, реже — половых органов. Помимо типичных элементов на слизистой отмечаются гиперемия и отёк, пузыри, эрозии и язвы. Пузыри могут образовываться и на фоне гипертрофических
очагов и бляшек на коже. Болеют преимущественно лица пожилого возраста с сопутствующими соматическими заболеваниями (чаще печени, желудочно-кишечного тракта). Для этой категории больных наиболее характерно хроническое течение дерматоза (торпидное или с частыми рецидивами, иногда протекающими остро). При остром течении почти всегда удается обнаружить связь с пероральным или парентеральным приемом лекарств. Характерен зуд. После разрешения сохраняются очаги инфильтрации, гиперпигментации, атрофии, дис-хромии, пойкплодермии, реже — фиброза и склероза.
Для разграничения лихенопдных реакций кожи и слизистых был создан определенный диагностический алгоритм, позволяющий врачу выбрать тактику ведения больного (обследование в амбулаторных условиях, терапевтическом стационаре, у стоматолога, назначение амбулаторного или стационарного лечения).
Для математической обработки использовали все 325 историй болезни. Составив ряд клинических критериев КПЛ, мы определили .встречаемость их в каждой из трех, образованных по факторам риска групп больных. В математизации симптомов был использован принцип альтернативного кодирования. Придание количественных значений клиническим симптомам проводилось при помощи алгоритма последовательного критерия отношения вероятностей, в соответствии с которым решение задачи сводится к отношению объекта (в данном случае больного) к одному из трех классов на основании частоты признаков. Из набора всех признаков с помощью коэффициента корреляции выбираются независимые. Вероятность симптома определялась отношением числа больных, имеющих данный симптом к общему числу больных в группе. По существу для дифференциальной диагностики важна не сама вероятность симптома, а вероятность отношения их вероятностей. В результате компьютерной обработки получены две группы автоматической системы, так как оказалось, что суммы (Э) количественных значений симптомов (Р) 1-й и 2-й групп больных (провоцирующие факторы экзогенного характера — вирус? и химические, лекарственные вещества, воздействующие .непосредственно на кожу) имеют приблизительно одинаковые значения. Таким образом, задача врача еще более упрощается. Заполнив таблицу (таблица 1) и определив сумму количественных значений признаков заболевания, врач решает задачу, в какую группу отнести больного. То есть врачу предлагается регламентированная
Вычислительная дифференциально-диагностическая таблица разграничения лихеноидиых реакций в зависимости от провоцирующего фактора (1 — экзогенного характера, II — эндогенного)
