Клинический дерматит у ребенка
Атопический дерматит у детей. Часть первая (Клиническая лекция) Текст научной статьи по специальности «Медицина и здравоохранение»
Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Федотов Валерий Павлович, Попович Юлия Александровна
На основании многолетних личных исследований и наблюдений, критического анализа значительного числа литературных источников, авторами доступно, целостно и методично изложен материал по проблеме атопического дерматита у детей. Уделено внимание проблеме эпидемиологии, этиологии и факторов риска дерматоза, неалергенным факторам, факторам, усугубляющим действие триггеров, иммунопатологии, классификации, диагностике заболевания, качеству жизни, клинике дерматоза.
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Федотов Валерий Павлович, Попович Юлия Александровна,
Atopic dermatitis in infants. First part. (A clinical lecture)
On the basis of own independent research and observations of many years, the critical analysis of a great deal of literary sources, the authors accessibly, integrally and methodically expounded an issue of the atopic dermatitis in infants. Considerable attention has been given to the problem of epidemiology, aetiology and risk factors of the dermatosis, to the anallergic factors, factors aggravating the triggers action, immunopathology, classification, diagnostics of the disease, the quality of life and clinic of the dermatosis.
Текст научной работы на тему «Атопический дерматит у детей. Часть первая (Клиническая лекция)»
Атопический дерматит у детей. Часть первая
Федотов В. П., Попович Ю. А.
Запорожский государственный медицинский университет
На основании многолетних личных исследований и наблюдений, критического анализа значительного числа литературных источников, авторами доступно, целостно и методично изложен материал по проблеме атопиче-ского дерматита у детей. Уделено внимание проблеме эпидемиологии, этиологии и факторов риска дерматоза, неалергенным факторам, факторам, усугубляющим действие триггеров, иммунопатологии, классификации, диагностике заболевания, качеству жизни, клинике дерматоза.
Ключевые слова: атопический дерматит, аллергия, иммунитет, аллергены, диагностика, клиника, осложнения.
В.1 Эпидемиология атопического дерматита у
В.2 Этиология и факторы риска развития
атопического дерматита. 157
В.2.1 Пищевые аллергены. 158
В.2.2 Бытовые аллергены. 159
В.2.3 Пыльцевые аллергены. 159
В.2.4 Бактериальные аллергены. 159
В.2.5 Грибковые аллергены.
В.2.6 Вакцинальные аллергены.
В.2.7 Эпидермальные аллергены.
В.3 Неаллергенные факторы.
В.3.1 Психоэмоциональные нагрузки.. В.3.2 Пищевые добавки.
В.3.3 Поллютанты. Метеоколебания. Ксенобиотики. .161
1 Факторы, усугубляющие действие триггеров..161
2 Иммунопатология атопического дерматита. 161
2.1 Гистопатология атопического дерматита. 162
2.2 Кожа как иммунный орган. 162
2.3 Нарушение барьерной функции кожи. 163
3 Атопический дерматит и качество жизни. 164
4 Классификация атопического дерматита. 164
5 Методы аллергологического обследования, используемые при атопическом дерматите. 165
6 Диагностика атопического дерматита. 165
6.1 Критерии диагностики. 165
6.2 Клиническая картина атопического дерматита. 166
7 Осложнения атопического дерматита. 167
8 Собственные исследования. 167
Атопический дерматит — хроническое рецидивирующее заболевание, характеризующееся высыпаниями, зудом и сухостью кожи. В 80 % случаев его впервые диагностируют у детей первых пяти лет жизни, у 73 больных заболевание персистирует во взрослом возрасте, у остальных — может спонтанно разрешиться.
Современными эпидемиологическими исследованиями установлено, что атопическим дерматитом страдает 10-20 % детей во всем мире; в 2-5 % случаев он начинается во взрослом возрасте; у 60-70 % взрослых пациентов в дальнейшем атопический дерматит трансформируется в экзему рук или профессиональные кожные заболевания.
У детей атопический дерматит нередко является первой клинической манифестацией «аллергического марша»: большинство из этих детей имеют высокий риск развития бронхиальной астмы, аллергического риноконъюнктивита. Так, 80 %
детей с атопическим дерматитом страдают аллергическим ринитом или бронхиальной астмой, и течения этих заболеваний у них более тяжелое.
Кардинальный признак атопического дерматита — зуд кожных покровов, который негативно влияет на все аспекты качества жизни; также значителен материальный ущерб от этого заболевания.
Представляет трудности диагностика ато-пического дерматита, особенно у детей раннего возраста; имеют значение морфологические особенности кожи и возраст больных.
Современные исследования подтверждают мультифакторный характер атопического дерматита, на инициацию которого существенное воздействие оказывают многочисленные генетические и средовые факторы.
Основные цели лечения атопического дерматита:
— уменьшение симптомов болезни;
— обеспечение длительного контроля над те-
Это достигается назначением адекватной терапии, а также тесным сотрудничеством между врачом, пациентом и ухаживающими за ним лицами, которых врач и медсестра параллельно изучают по специальной программе.
В.1 Эпидемиология атопического дерматита у детей. Атопический дерматит — генетически детерминированное заболевание кожи с неясным до конца этиопатогенезом.
Современные эпидемиологические исследования атопических заболеваний основаны на изучении следующих показателей:
— распространенность — процент лиц, страдающих заболеванием, расстройством или нарушениями в популяции (кумулятивная распространенность — общее количество больных, выраженное как процент популяции, в которой развилось расстройство к определенному времени; точечная распространенность — это процент популяции с расстройствами в определенный момент времени);
— заболеваемость — количество лиц, заболевших в течение определенного периода времени (обычно в течение года), выраженное в процентах от всей популяции;
— болезненность — влияние степени заболевания (госпитализации и др.) на качество жизни человека;
— атопия — склонность, обычно генетическая, к развитию (иммуноглобулин £)-зависимого ответа на воздействие распространенных аллергенов окружающей среды.
За последние полвека в промышленно развитых странах распространенность атопических заболеваний у детей возросла на 30-50 %. Существенный рост заболеваемости атопическим дерматитом отмечен в Японии, США, странах Африки, Великобритании, Италии, Австралии, Северной Европе.
Самый низкий показатель распространенности атопического дерматита характерен для Азии (5 %).
Хотя в развитии атопического дерматита важное значение придают генетической отяго-щенности, различия в распространенности заболевания как между, так и внутри различных стран доказывают неоспоримое влияние неизвестных внешних факторов окружающей среды. Например, после объединения Германии атопический дерматит чаще встречался среди детей, проживающих в Западной Германии,
чем в «загрязнённом» Лейпциге. В качестве потенциальных факторов риска, которые могли способствовать более высокой манифестации неаллергического типа атопического дерматита среди детей, ученые рассматривают инфекции, питание, поллютанты. Различие в распространенности атопического дерматита в Великобритании они связывают с более высокой температурой и влажностью воздуха в южной части страны, что способствует усиленному размножению клещей и повышению их концентрации в воздухе. Установлено, что дети, проживающие в сельской местности, страдают атопическим дерматитом реже, тогда как дети из маленьких семей с высоким социально-экономическим статусом, напротив, болеют чаще.
При обследовании детей в г. Москва и Московской обл. в течение трех лет показано рост заболеваемости атопическим дерматитом с 4,9 % в 1997 г. до 6,7 % в 2000 г.
В целом в России и Украине отмечается рост заболеваемости атопическим дерматитом, особенно тяжелыми формами.
Ряд авторов указывают на несколько важных концепций в эпидемиологии атопического дерматита:
— во-первых, нет убедительных данных, подтверждающих наличие обратной связи между частотой инфекций и риском развития атопиче-ского дерматита;
— во-вторых, риск развития бронхиальной астмы у детей с ранним началом атопического дерматита не высок, поскольку при рассмотрении вопроса об «аллергическом марше» важен фенотип заболевания, а не прогрессирование самого «аллергического марша».
Проведение эпидемиологических исследований способствует лучшему пониманию патофизиологических механизмов заболеваний, а полученные результаты могут составить в будущем основу превентивной терапии и разработки профилактических мероприятий.
В.2 Этиология и факторы риска развития атопического дерматита. Многочисленные исследования показали, что атопический дерматит представляет собой комплексное генетическое заболевание. Если оба родителя страдают каким-либо атопическим заболеванием, то риск развития атопического дерматита у ребенка составляет 75 %, если один из родителей, то риск — 50 %, а у здоровых родителей — 10-20 %. Развитие ато-пического дерматита у ребенка больше связы-
вают с атопическим статусом матери, чем отца. Одним из факторов риска развития атопии у новорожденного ребенка считают низкий уровень IL-13, ингибирующего продукцию противовоспалительных цитокинов из моноцитов. Кроме того, IL-13 влияет на пролиферацию 5-клеток, включая синтез IgE, тормозит выработку IL-12 и активацию Th 1-лимфоцитов.
Последние исследования в области генетики доказывают связь атопического дерматита с полиморфизмом гена ß-цепи рецептора IgE и мутацией а-цепи рецептора IL-4; изучается также возможная роль хромосомы 3g21. Недавно установлено, что наиболее чувствительный ло-кус атопического дерматита расположен на хромосомах 1g21, 17g25, 20р.
Сенсибилизация организма происходит на уровне кожи. Хотя воспалительный процесс при атопическом дерматите локализован в коже, IgE, эозинофилы и Тй2-клетки, в силу своей специфической циркулирующей способности, могут перемещаться в очаг воспаления. Экспериментально было доказано, что эпикутанная сенсибилизация аллергеном овалобумина приводит к развитию дерматита у мышей и способствует продукции IgЕ.
Некоторые ученые высказывают мнение об аутоиммунном компоненте атопического дерматита. Считают, что ксероз, зуд, дисгидроз, ихтиоз, бактериальные и вирусные инфекции способствуют высвобождению из поврежденной ткани и кератиноцитов аутоаллерге-нов, которые являются триггером IgE- или Т-клеточного ответа. IgE-антитела к аутоанти-генам могут активировать дендритные клетки и индуцировать пролиферацию аутореактивных Т-клеток. Аутореактивность развивается в первые годы жизни ребенка в виде сенсибилизации к пищевым и респираторным аллергенам. Удалось выделить из сыворотки большинства больных с тяжелой формой атопического дерматита IgE-реактивные аутоантигены, направленные против человеческих протеинов, и даже клонировать участок комплементарного ДНК из кератиноцитов кожи; причем уровень IgE-аутоаллергенов снижается в результате успешного лечения атопического дерматита.
Исключительно грудное вскармливание в течение, по крайней мере, первых четырёх месяцев жизни является защитным фактором и находится в обратной зависимости с развитием атопического дерматита у младенцев; это может длиться до трёх лет.
Атопический дерматит чаще диагностируется у детей, чьи матери имеют высшее образование, а также в семьях с высоким социальным статусом. Доказано, что внутриутробные инфекции, а также 2-3 курса антибиотиков, принимаемые матерью во время беременности, представляют потенциальный риск возникновения атопического дерматита у ребенка.
Играет определенную роль в возникновении атопического дерматита загрязнение окружающей среды и экспозиция ингаляционных аллергенов, применение центральных отопительных систем, двойное остекление окон и наличие ковров.
Заболевание атопическим дерматитом может быть классифицировано как аллергическое, так и как неаллергическое. В качестве экзогенных этиологических факторов рассматриваются:
— аллергенные (ингаляционные, пищевые) раздражители:
Атопический дерматит: как и чем помочь ребенку?
Сухая кожа, красные щечки, отеки, сильное беспокойство и неутихающий плач — вот что видят родители ребенка с атопическим дерматитом.
Младенец не может объяснить, что его беспокоит, и лишь криком дает понять, что ему некомфортно и плохо. Пожалеть малыша, защитить и помочь — первое желание близких в этот период. Но лечить атопический дерматит у детей гораздо труднее, чем попытаться предотвратить заболевание. Поэтому Мedportal.ru рассказывает о том, какой должна быть профилактика атопического дерматита с рождения.
Врач, поставивший ребенку этот диагноз, расскажет родителям о том, как лечить атопический дерматит, и что это хроническое заболевание аллергической природы. Он не заразен и может долгое время не проявляться. Но когда обостряется атопический дерматит, симптомы его не самые приятные: постоянный зуд, мокнущие расчесы по всему телу, шелушение кожи мешают спать, играть и развиваться.
Откуда это взялось?
Мамы детей с атопическим дерматитом часто винят в болезни себя: свой образ жизни во время беременности или диету при кормлении. Они переживают, что ребенку придется жить в особых условиях: например, не ходить в сад из-за обострений болезни или есть только определенные неаллергенные продукты. К страхам за здоровье малыша прибавляются опасения, что из-за заболевания придется перестраивать всю жизнь семьи. Выйдет ли мама на работу, когда придет время? Сможет ли семья поехать отдыхать? Не испортятся ли отношения родителей ребенка? Не на все эти вопросы может ответить врач, но он, как хороший специалист, успокоит родителей: прямой вины мамы в том, что ребенок заболел, нет. Съеденный в беременность гамбургер или выпитая бутылка газировки не причина детских страданий. Основной фактор заболевания — наследственность. Если атопический дерматит есть у обоих родителей, болезнь передастся ребенку в 50-80% случаев. Если же болеет только папа или мама, можно говорить о 40-50% [1,2] вероятности заболевания.
За последние 16 лет количество детей с атопическим дерматитом увеличилось вдвое: помимо наследственного фактора, на детское здоровье влияют воздух больших городов и жесткая вода, аллергены, которых становится все больше; еда, транспорт — все то, что есть в мегаполисах с избытком. Именно по этой причине в деревнях атопический дерматит встречается крайне редко. Родителям нужно учесть все эти факторы и проявить настороженность: если кожа ребенка склонна к атопии, нужна профилактика! Клинические проявления можно и нужно предотвратить.
В чем особенности кожи, склонной к атопии?
Если кожа малыша очень сухая, шершавая, даже шелушащаяся; ребенок чешется так, что не может уснуть; а на локтях, под коленями, на тыльной стороне рук, шее, на лбу или на щеках появляются симметричные красные пятна, значит, у него есть признаки склонности к атопическому дерматиту. И родителям сразу нужно проконсультироваться с педиатром. Такой коже требуется защита и укрепление гидролипидного слоя: из-за недостатка липидов аллергены проникают внутрь эпидермиса и вызывают воспаление.
Профилактика лучше лечения
Для мамы, которая столкнулась со вспышкой атопического дерматита у ребенка, назначение гормональных мазей дерматологом всегда звучит как приговор. Поэтому во избежание применения глюкокортикостероидных средств необходимо ввести в ежедневную практику ухода за кожей использование кремов-эмолентов.
Эмоленты — вещества, увлажняющие кожу и способные удерживать влагу, закрепляясь в роговом слое. Как правило, при первых признаках педиатр назначает ежедневный профилактический уход за кожей кремами-эмолентами. Крем поможет поддержать нормальное состояние кожи во время ремиссии и сократят риск появления обострений. Но крем при атопическом дерматите нельзя использовать, когда на коже уже появляются мокнущие участки.
Ученые из Великобритании и Японии в 2014 году доказали, что ежедневное использование эмолентов у детей с рождения снижает риск развития клинических признаков атопического дерматита на 30-50% [3,4].
Как выбрать правильный крем при атопическом дерматите?
При выборе косметики для ребенка-атопика стоит обратить внимание на следующие критерии:
БЕЗОПАСНОСТЬ С РОЖДЕНИЯ. Профилактику у детей с наследственным фактором необходимо начинать как можно раньше. Если вы знаете, что у вас или супруга когда-либо был атопический дерматит или бывают аллергические реакции, в том числе аллергический ринит, то при выборе средств ухода за ребенком нужно отдавать предпочтение средствам для склонной к атопии кожи. Но не все средства для ухода за склонной к атопии кожи можно применять с рождения, поэтому выбор лучше делать в пользу проверенных детских брендов, продающихся в аптеках. Например, средства серии «STELATOPIA» от французского бренда Mustela разрабатывались с участием дерматологов и педиатров специально для детей с рождения. Это линейка создана как раз для склонной к атопии кожи.
ГИПОАЛЛЕРГЕННОСТЬ. Слабый кожный барьер склонной к атопии кожи не может в полной мере препятствовать проникновению аллергенов, отчего и бывает воспаление. Поэтому средства для ухода за такой кожей должны быть гипоаллергенны и лучше, чтобы в них не было сомнительных ингредиентов, таких как парабены, фталаты, феноксиэтанол, а также отдушек. Стоит отметить, что 100% натуральный состав не всегда гарантирует гипоаллергенность, так как некоторые природные эфирные масла могут стать причиной аллергических реакций. Если есть сомнения, то лучше проконсультироваться с педиатром или фармацевтом.
ДОКАЗАННАЯ ЭФФЕКТИВНОСТЬ. Использование смягчающего крема или бальзама в первую очередь должно помочь уменьшить дискомфорт у малыша, вызванный чрезвычайной сухостью кожи. Выбирайте средства, которые прошли клинические испытания и доказали свою эффективность при уходе за детской кожей. Так, компания Laboratoires Expanscience оценила эффективность применения средств MUSTELA STELATOPIA у детей первого года жизни. В течение 9 месяцев ученые клинически обследовали 113 новорожденных, у которых риск клинического проявления атопического дерматита составлял 50-80%, т.е. оба родителя перенесли атопический дерматит. Первая группа детей (60 детей) получала программу ухода за кожей MUSTELA «STELATOPIA» (смягчающий бальзам, крем для купания или масло для ванны), а 53 ребенка не получали специфического ухода за кожей. Результаты показали, что ежедневное использование программы ухода “STELATOPIA” один раз в день в течение 9 месяцев позволило снизить вероятность клинического проявления атопического дерматита у детей на 51%.
КОМПЛЕКСНЫЙ УХОД. Выбирая смягчающий крем при атопическом дерматите для ребенка, важно учесть и тот факт, что средство для купания также должно отвечать требованиям к уходу за склонной к атопии кожей: в нем не должно быть мыла (так как мыло сушит кожу и нарушает целостность гидролипидной пленки), в средстве нежелательно присутствие сульфатов (так они могут очень агрессивно воздействовать на, и без того сухую, кожу ребенка). Хорошо, если средство содержит липидовосстанавливающие компоненты. Желательно, чтобы крем и средство для купания были из одной линейки, чтобы обеспечить оптимальный комплексный уход.
В наших силах помочь малышу поддерживать кожу здоровой и вести полноценный образ жизни. Защищайте склонную к атопии кожу с рождения, и вашего малыша не будут беспокоить зуд и сухость кожи.
Атопический дерматит у детей
В отечественной и зарубежной литературе проблеме атопического дерматита (АД) посвящены сотни статей и монографий. Несмотря на столь пристальное внимание к данной проблеме, следует констатировать и рост числа больных, страдающ
В отечественной и зарубежной литературе проблеме атопического дерматита (АД) посвящены сотни статей и монографий. Несмотря на столь пристальное внимание к данной проблеме, следует констатировать и рост числа больных, страдающих АД, и недостаточную эффективность используемых методов лечения. На сегодняшний день отсутствует общепризнанное определение данного заболевания.
АД (атопическая экзема, синдром атопической экземы/дерматита) — хроническое аллергическое воспалительное заболевание кожи, сопровождающееся зудом, возрастной морфологией высыпаний и стадийностью [1]. В определении АД, приведенного в согласительном документе Ассоциации детских аллергологов и иммунологов России, подчеркивается еще и гетерогенность механизмов, участвующих в формировании данного заболевания.
АД является хроническим аллергическим лихенифицирующим воспалением кожи, возникающим в результате готовности иммунной системы к развитию аллергической реакции, способной быть запущенной как атопическими, так и неатопическими механизмами. Сопровождается зудом и частым инфицированием [3].
Достижения иммунологии с середины 90-х годов прошлого столетия привели к пониманию сути основных изменений, происходящих у некоторых больных с аллергическим поражением кожи. Признание главенствующей роли атопии в генезе нескольких вариантов аллергического дерматита привело к попытке объединения их в диагнозе АД. Диагноз АД объединил ранее существующие диагнозы, такие как «нейродермит», «диатезное пруриго», «пруриго Бенье», «эндогенная экзема», «экссудативный экзематоид», «астма-экзема», «конституциональная экзема», «экссудативный диатез», «аллергический диатез», «детская экзема», «истинная экзема», «пеленочный дерматит» и многие другие. Следует признать, что некоторые из перечисленных терминов до настоящего дня используются в Европе. Это существенно затрудняет проведение эпидемиологических исследований с целью выяснения истинного числа больных детей, страдающих АД. По результатам стандартизированного международного эпидемиологического исследования ISAAC (Internetional Study of Asthma and Allergy in Childhood — международное исследование астмы и аллергии у детей) распространенность АД у детей в США достигла 17%, в Европе — 15,6%, в Российской Федерации составила от 6,2% до 15,5%. Отмечается постоянная тенденция к росту числа больных детей, страдающих АД, в мире [3].
Согласно основополагающим документам Европейской комиссии по номенклатуре заболеваний (2002, 2004) существуют пациенты с «атопической экземой/дерматитом», у которых имеет место IgE-зависимый механизм, и больные, у которых нет данных за IgE-зависимый механизм (рис. 1).

В то же время в современной западной дерматологии «атопия» — это клинический диагноз, и заболевание может называться «атопическим» даже без подтверждения кожными тестами или присутствия IgE-антител в его сыворотке. Большинством экспертов Европейской комиссии по номенклатуре заболеваний признается необходимость создания нового термина для «атопической экземы/дерматита».
В нашей стране существует рабочая классификация АД, предложенная РААКИ (Российской ассоциацией аллергологов и клинических иммунологов) в 2002 году. К сожалению, практикующие врачи редко используют ее в своей работе, ограничиваясь указаниями лишь на период ремиссии или обострения заболевания (табл. 1).
По мнению большинства исследователей АД следует относить к мультифакторным заболеваниям с полигенным типом наследования с пороговым эффектом. При сочетании определенных генетических дефектов и средовых факторов достигается пороговое значение, при котором и появляется клиническая картина заболевания. Существует большое количество фенотипически здоровых людей с высоким риском формирования аллергических заболеваний в неблагоприятных условиях внешней среды.
При выраженных наследственных дефектах достаточно воздействия незначительных средовых факторов, чтобы очень быстро предрасположенность к развитию аллергического заболевания реализовалась в виде заболевания. И наоборот, агрессивные факторы внешней среды даже при минимальных генетических дефектах могут привести к быстрому формированию АД.
Достижения фундаментальных научных исследований в области молекулярной медицины привели сегодня к пониманию сути биологических дефектов, происходящих у больных с АД.
В современной литературе собрано большое количество наблюдений, указывающих на связь аллергических заболеваний у родителей или родственников больного с появлением каких-либо аллергических проявлений у детей. Если оба родителя ребенка страдают атопическим заболеванием, то риск формирования АД по разным данным составляет от 50% до 80%, если наследственность отягощена по материнской линии, то риск развития аллергического (атопического) заболевания составляет от 30% до 50% [12].
В настоящее время описано более 20 генов-кандидатов, ответственных за формирование АД. Уже в 21 веке описали 13 новых полиморфизмов, связанных с формированием аллергического поражения кожи, расположенных главным образом на хромосомах 1q, 3q и 17q.
Учитывая достижения современной молекулярной медицины, можно выделить несколько групп кандидатных генов, контролирующих возможность формирования АД.
Предрасположенность к атопии связывают преимущественно с локусами 1q23-q25, 13q14.1, 11q12-q13, 6p21.2-p12, 5q33.2, 5q32 (табл. 2).
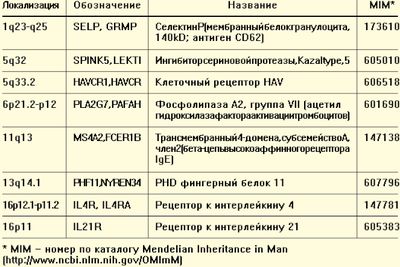
Безусловно, основным, но не единственным механизмом формирования АД следует признать аллергические реакции 1-го типа (атопические, типа анафилаксии) по классификации Джелла и Кумбса. Какие бы типы аллергических реакций не принимали участие в формировании данного заболевания, ключевым звеном патогенеза АД является выработка у этих больных провоспалительных цитокинов и хемокинов, ответственных за формирование хронического аллергического воспаления. Это в первую очередь IL-4 и рецептор к IL-4, IL-5, IL-6, IL-10, IL-13, IL-18, TGF-бета1 (трансформирующий фактор роста-бета), TNF-альфа (фактор некроза опухоли-альфа), GM-CSF (грануляцитарно-макрофагальный колониестимулирующий фактор), IFN-гамма (интерферон-гамма). Для полноценной аллергической реакции необходимо формирование большого количества хемокинов, ответственных за хемотаксис моноцитов, базофилов (CCL2), индуцирование и привлечение (CCL11 или Eotaxin) в место аллергической реакции эозинофилов, выделения содержимого гранул эозинофилов (CCL5 или RANTES) [8]. Кожа больных с АД отличается особой сухостью и ранимостью. Одним из механизмов предрасположенности к изменению барьерной функции кожи являются изменения в гене, кодирующем белок — филаггрин (filaggrin). Лица с мутациями в гене, кодирующем filaggrin, предрасположены к формированию вульгарной формы ихтиоза и синдрома атопической экземы/дерматита. Filaggrin — защитный белок, который обычно экспрессируется в клетках кожи. Он действует как физический барьер, препятствующий воздействию потенциально опасных веществ из окружающей среды. Ученые выдвинули гипотезу, что наследование одного или двух дефектных генов filaggrin может ослаблять этот физический барьер, снижая его эффективность, и тем самым повышать риск формирования аллергического поражения кожи [10, 11, 13].
Клинические проявления АД у детей, как правило, появляются на первом году жизни в виде экссудативного типа кожного поражения. В первую очередь страдает лицо, шея, туловище и разгибательные поверхности конечностей. Существует мнение, что у больных с АД имеет место стадийность в типах кожного поражения. Начинается в виде младенческой формы, затем формируется детская и завершается взрослым типом. У некоторой части больных такая эволюция клинической картины может иметь место. Однако у многих больных одновременно отмечаются как типичные признаки младенческой формы (экссудативный тип поражения), так и лихеноидные высыпания в естественных складках кожи. Предлагается выделять экссудативную, эритематозно-сквамозную и лихеноидную формы АД [2, 4].
При экссудативной форме АД в периоде обострения заболевания выявляется гиперемия, отек кожи, папулы, везикулы, эрозии и мокнутия. Обычно первые элементы появляются на лице, чаще симметрично, и сопровождаются сильным зудом. Постепенно процесс распространяется на ранее неизмененные участки кожи, пузырьки вскрываются, образуя большую эрозивную поверхность, покрытую в дальнейшем корками. На лице в первую очередь страдают щеки, лоб и волосистая часть головы. Аналогичные изменения могут появляться и в естественных складках (локтевые, подмышечные и ягодичные области).
При эритематозно-сквамозной форме АД в периоде обострения у больных появляются эпидермодермальные папулы, сопровождающиеся сильным зудом и как следствие этого появлением у больных расчесов на фоне сухости кожи.
При преобладании в клинической картине заболевания лихеноидной формы АД в фазе обострения отмечается инфильтрация и лихенификация кожи на фоне эритемы и умеренного отека. Отмечается, как правило, выраженная сухость кожных покровов и признаки лихенификации — утолщение и усиление кожного рисунка. Процесс в основном сконцентрирован в естественных складках и сгибах. Основным элементом при данной форме АД являются эпидермодермальные папулы, склонные к слиянию. У больных отмечается сухость кожных покровов, шелушение и зуд. Постепенно с прогрессированием процесса возникает гиперпигментация в месте воспаления и трещины.
При остром течении АД преобладает, как правило, экссудативный компонент воспаления, что сопровождается выраженным отеком кожи, гиперемией и мокнутием.
В подостром периоде АД отмечается постепенное уменьшение отека, гиперемии и мокнутия. При лихеноидной форме заболевания выявляется очаговая инфильтрация, лихенификация, сухость и шелушение кожи. На месте очагов воспаления возможно появление участков депигментации.
У больных с пруригоподобной формой заболевания появляются множественные изолированные плотные папулы, на вершине которых выявляются мелкие везикулы. Эти высыпания появляются на фоне лихенифицированно измененной кожи, чаще в области естественных складок и сгибах. Следует подчеркнуть, что основным проявлением заболевания является интенсивный зуд.
В периоде неполной ремиссии заболевания у больных АД сохраняются минимальные проявления в виде очагов шелушения, сухости, единичных экскориаций. В период полной ремиссии могут отмечаться шелушение, сухость и очаги гипер- или гипопигментации, признаки атрофии кожи. Для оценки степени тяжести кожного процесса в нашей стране принято использовать индекс SCORAD (1993). Этот коэффициент позволяет объективно оценить степень тяжести заболевания, однако в практической работе редко используется. В практической работе врачи опираются на следующие критерии тяжести:
Легкое течение заболевания характеризуется незначительной гиперемией, экссудацией и шелушением. У больных появляются единичные папулы и везикулы. Зуд слабый и сопровождается единичными расчесами. Сон не нарушен. Реакции региональных лимфоузлов нет.
Среднетяжелое течение заболевания проявляется множественными очагами поражения кожи с выраженной экссудацией и/или лихенификацией. У больных отмечается умеренный зуд и расчесы. Выявляется умеренное увеличение региональных лимфоузлов.
Тяжелое течение характеризуется диффузными изменениями кожных покровов, выраженной экссудацией и/или лихенификацией, эрозиями. Отмечается мучительный зуд, нарушающий общее самочувствие. Реакция всех групп лимфатических узлов. Особенно тяжелое течение заболевания наблюдается у детей с поражением кожи в виде эритродермии, требующей, как правило, назначения системных глюкокортикоидов.
Диагностические критерии АД
По мнению большинства специалистов, диагноз АД базируется на клинических признаках, так как нет ни одного лабораторного или иного критерия, который бы сразу верифицировал данное заболевание. Как не существует общепринятого определения этого заболевания, так и не существует единых критериев постановки диагноза. Хорошо известны критерии АД J. M. Hanifin и G. Rajka (1980), выделивших 4 главных критерия и более чем 20 дополнительных. Для верификации диагноза требовалось, по крайней мере, по 3 критерия из обеих групп [9]. В 1994 году эти критерии были пересмотрены в Лиллехамере (Норвегия) с целью минимизации признаков. Однако и эти критерии не нашли широкого применения в повседневной работе врача-педиатра.
Достаточно привлекательными выглядят критерии, разработанные экспертами в Великобритании и представленные в виде Согласительного документа «Атопическая экзема у детей» в декабре 2007 [7]. АД должен быть диагностирован, когда у ребенка есть кожный зуд плюс три или более из следующих признаков:
Чувствительность данного набора критериев составила 85%, а специфичность — 96% [10].
В 2008 г. опубликованы диагностические критерии АД в клинических рекомендациях для педиатров в разделе аллергология и иммунология под редакцией академиков А. А. Баранова и Р. М. Хаитова (табл. 3).
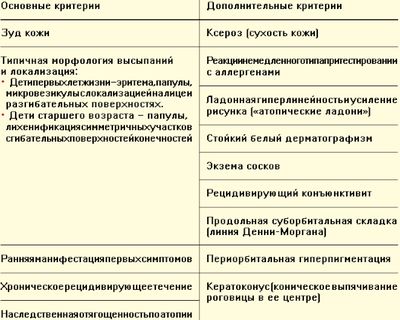
Дополнительные критерии помогают заподозрить АД, но не являются специфическими.
Таким образом, диагностика АД базируется на основных клинических признаках: наличие дерматита с типичной локализацией (в зависимости от возраста), распространенным зудом и сухостью кожных покровов. При наличии сопутствующего аллергического поражения респираторного тракта (аллергический ринит, бронхиальная астма), со сходным атопическим механизмом, естественно предположить, что и кожные проявления имеют аналогичный иммунный дефект. Большое диагностическое значение имеют: отягощенная наследственность по атопическим заболеваниям, прямые или косвенные признаки, указывающие на связь обострения дерматита с неинфекционными аллергенами (пищевыми, эпидермальными, пыльцевыми) и положительный эффект элиминации.
Лабораторные и специальные методы диагностики
Исследование уровня общего и аллергенспецифичных IgE имеет важное значение у больных с АД. Особенно важно это исследование у больных с пищевой аллергией, проявляющейся в виде АД. Определение IgE специфических антител позволяет выявить основные неинфекционные аллергены, вызывающие обострение АД. Однако следует учитывать, что отсутствие IgE-антител не исключает атопический характер заболевания. Бывают ложноотрицательные результаты данного тестирования, особенно часто выявляемые у детей первых двух-трех лет жизни. Не следует забывать, что причинными для детей с АД могут быть и ингаляционные аллергены (домашняя пыль, клещи домашней пыли Dermatophagoides pteronyssinus или Dermatophagoides farinae, эпидермальные аллергены и пыльца растений, грибковые аллергены). Появление обострения АД у детей после контакта с домашними животными, шерстяными или меховыми изделиями, ухудшение течения заболевания в весенне-летний период — все это указывает на возможность сенсибилизации к неинфекционным аллергенам. Иногда бывает вполне достаточно исключить из окружения больного с АД домашних животных, поменять «пуховик» на одежду из современных синтетических материалов, и у больного уменьшаются или вообще купируются все клинические проявления АД. Поэтому вопросам диагностики сенсибилизирующих факторов следует уделять особое внимание. Патогенетически необоснованным выглядит попытка выявления сенсибилизации у больных с АД с помощью определения IgG-антител. Большинство антител класса IgG (возможно, кроме IgG4) относятся к блокирующим антителам и не имеют никакого диагностического значения.
В последние годы все большее внимание стали уделять диагностике бактериальной и грибковой сенсибилизации у больных с АД. Определение антител класса Е к Staphylococcus aureus и его экзотоксинам у больных с АД позволяет ряду специалистов предположить патогенетическое значение этого фактора. Тем более что у подавляющего числа больных с обострением АД обнаруживают стафилококковое обсеменение как пораженных, так и непораженных участков кожи [5]. Этих данных пока недостаточно, чтобы окончательно сделать вывод о значение IgE-антител к St. aureus в патогенезе АД.
Нельзя считать до конца решенными и споры вокруг значения определения IgE-антител к некоторым грибковым аллергенам. Чаще всего обнаруживаются грибы Malassezia furfur (Pityrosporum ovale и Pityrosporum orbiculare) у больных с АД [6]. Данный дрожжевой гриб заселяет кожу всех людей, и роль и значение его в патогенезе АД пока остаются неясными.
Другим методом диагностики неинфекционной сенсибилизации у больных АД является постановка кожных проб (тест уколом, кожно-скарификационные тесты, аппликационные тесты). Метод кожного тестирования хорошо себя зарекомендовал при диагностике бытовой и пыльцевой сенсибилизации. В диагностике пищевой сенсибилизации данный метод обследования занимает более скромное место. Большая частота ложноотрицательных и значительно реже встречающихся ложноположительных результатов предполагает необходимость проведения элиминационно-провокационных тестов, особенно важных для подбора индивидуальной диеты.
«Золотым стандартом» диагностики пищевой аллергии является двойная слепая плацебо-контролируемая проба. Обследуемому больному после периода элиминации вводят в питание проверяемый продукт в замаскированном виде. Кроме того, пациент получает и плацебо. При этом ни пациент, ни его родители не знают, что именно в данный момент вводится в питание. К сожалению, проведение провокации по вышеописанной схеме проводится только с научно-исследовательской целью. В практике врача-аллерголога встречается открытый пищевой провокационный тест, когда и пациент и его родители знают, какой конкретно пищевой продукт вводится больному. В ходе проведения провокации у пациента фиксируются клинические проявления обострения АД.
Дифференциальный диагноз следует проводить с большим кругом кожных, инфекционных, метаболических, неопластических и иммунодефицитных заболеваний (табл. 4).

Лечение
Современная стратегия лечения АД должна включать следующие направления (рис. 2):
У детей первого года жизни, страдающих АД, дебют заболевания чаще всего связан с пищевой аллергией. Постепенно с возрастом связь обострения АД с приемом пищевого аллергена не всегда прослеживается, в связи с чем значение строгой элиминации у больных АД детей старшей возрастной группы ставится под сомнение. Основная проблема в данном случае связана с недостаточно эффективными лабораторными методами диагностики пищевой аллергии, широко используемыми в практике. Следует еще раз подчеркнуть необходимость выявления всех причинных факторов, приводящих к формированию и обострению АД. Это в полной мере касается элиминационных диет, используемых у больных с пищевой аллергией, проявляющейся в виде АД. Нормализация диеты кормящей матери, использование при необходимости гидролизатов коровьего молока высокой степени, аминокислотных смесей позволяют добиться полной пищевой элиминации у большинства детей первого года жизни. Не следует забывать, что сенсибилизация у детей возможна при употреблении любого продукта питания (злаки, овощи, мясо, фрукты). Попытка частичной элиминации неэффективна и в большой степени вредна.
Элиминационные меры касаются не только пищевых аллергенов, но и бытовых и пыльцевых аллергенов. Устранение контакта больного ребенка с домашними животными, изделиями из шерсти, некоторых синтетических тканей и меха может существенно уменьшить клинические проявления АД. Создание гипоаллергенной диеты и быта — это необходимые условия достижения ремиссии АД у детей.
Учитывая патогенетические механизмы формирования АД, наружная (топическая) терапия абсолютно необходима каждому больному. Стандартная схема местной терапии АД включает противовоспалительные (гормональные и негормональные) средства и средства, относящиеся к так называемой лечебной косметике, восстанавливающие барьерные функции кожи.
Из наружных глюкокортикостероидов (ГКС) у детей следует применять препараты, обладающие минимальными побочными эффектами, при сохранении высокой степени противовоспалительного действия. В настоящее время в педиатрической практике чаще всего используются препараты последнего поколения — метилпреднизолона ацепонат (Адвантан), алклометазона дипропионат (Афлодерм) и мометазона фуроат (Элоком). Наружные ГКС назначают, как правило, короткими курсами с последующим переходом на нестероидные местные препараты. Следует с осторожностью назначать местные ГКС на чувствительные участки кожи и использовать только средства, относящиеся к 1 классу активности. При тяжелых обострениях АД возможно использование местных ГКС, относящихся к 3 классу активности (сильные) на туловище и конечностях. В случае присоединения бактериальных осложнений используют комбинированные препараты, содержащие местные ГКС, антибактериальные и противогрибковые препараты (Тридерм, Пимафукорт).
Пимекролимус (Элидел) — препарат из класса макролактамов, производное аскомицина. Пимекролимус связывается с молекулой макрофилина-12, что приводит к блокаде проведения внутриклеточного сигнала и подавлению синтеза провоспалительных цитокинов (IL-2, 3, 4, 5, IFN-гамма). Пимекролимус в форме 1% крема используется 2 раза в день. Особым преимуществом пимекролимуса следует считать возможность использования его на всех без исключения пораженных участках кожи. В связи с недоказанной безопасностью при длительном применении (> 1 месяца) ингибиторы кальциневрина признаны препаратами второй линии терапии АД, в то время как топические ГКС — препаратами первой линии [8].
В этом отношении представляют интерес препараты линии Скин-кап, которые содержат в качестве основного действующего вещества активированный пиритион цинка 0,2% в креме и аэрозоле и 1% в шампуне. Пиритион цинка — это комплексное органическое соединение цинка, практически нерастворимое в воде и стабильное в диапазоне рН 4,5–9,5. При изготовлении препаратов линии Скин-кап используются физико-химические методы активации цинка путем воздействия электромагнитного поля. Скин-кап оказывает выраженное противовоспалительное, антибактериальное и противогрибковое действие. Аэрозоль и крем Скин-кап разрешены к применению у детей с первого года жизни.
АД требует особого ухода за кожей как в период обострения заболевания, так и в период ремиссии. Основной целью общего ухода за кожей является гидратация кожи и восстановление барьерной функции. Регулярное использование смягчающих/увлажняющих средств имеет чрезвычайно важное значение для кожи. Входящие в состав увлажняющих средств эмульсификаторы влияют на барьерную функцию кожи, а церамидсодержащие липидные компоненты снижают трансэпидермальную потерю воды через кожу. В целом увлажняющие средства делают атопическую кожу менее чувствительной к ирритантам. В последнее время для уменьшения сухости кожи у пациентов, у которых применение смягчающих и увлажняющих средств оказалось малоэффективным, разработана новая линия препаратов, способных влиять на внеклеточную мембрану эпидермиса, — так называемые церамиддоминирующие смягчающие средства [3].
Для ухода за кожей существуют различные средства лечебно-косметической серии типа Мустела СтелАтопия (Mustela), Авен (Avene), А-Дерма (A-Derma), Топикрем (Nigy Charlieu), Виши (Vichy), Урьяж (Uriage), Биодерма (Bioderma). Для устранения сухости кожи используют также Бепантен, F-99, Драполен, крем Унна. К наружной терапии относят также препараты, содержащие антигистаминные средства (Фенистил гель).
Прурисед крем (Uriage) представляет собой эмульсию «вода в масле». Содержит 8% каламина, линолевую и гамма-линоленовую кислоты. Оказывает быстрое успокаивающее, противозудное действие (2 часа), прогрессивно уменьшает частоту приступов зуда. Вся косметическая линия Урьяж (Uriage) создана на основе целебных термальных вод и удовлетворяет всем основным потребностям кожи у больных с АД. Термальная вода Урьяж (Uriage) — природная изотоническая вода, содержащая уникальную концентрацию минеральных элементов, нейтральный pH, и поэтому прекрасно увлажняет, защищает и успокаивает кожу.
Для смягчения и увлажнения кожи больных с АД используют: Топикрем, Липикар бальзам, эмульсия Липикар; Мустела СтелАтопия крем-эмульсия, успокаивающий крем А-Дерма. В период обострения заболевания — крем Атодерм P. O. цинк, линия Трикзера, линия А-Дерма Эгзомега и другие. В период ремиссии заболевания используют: Топикрем, Мустела СтелАтопия крем-эмульсия, крем Атодерм, Урьяж Cu-Zn-гель, Авен Трикзера, А-Дерма Эгзомега, Иктиан крем.
Активное использование в последние годы местной ГКС-терапии позволило добиться более легкого течения обострения заболевания. Это, безусловно, глобальное достижение. Однако формирование длительной ремиссии заболевания, без опасности развития побочного действия медикаментозной терапии, крайне затруднительно. Одна из главных причин недостаточного эффекта проводимой терапии это попытка «забыть», что АД — это гетерогенное заболевание. Гетерогенность АД касается в первую очередь этиологии и патогенеза заболевания. Гетерогенность эволюции данного заболевания (особенно ярко прослеживаемая у детей), обусловленная различными патогенетическими формами заболевания, подразумевает использование различных подходов к профилактике и лечению АД у детей.
