Лечение плоского лишая в полости рта
Иммунокоррегирующая терапия красного плоского лишая слизистой полости рта Текст научной статьи по специальности «Медицина и здравоохранение»
Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Сапарова Г.А.
Полиоксидоний в комплексном лечении больных красным плоским лишаем способствуют восстановлению, как местной защиты полости рта, так и общей системы иммунитета, ускоряет сроки заживления и снижает число рецидивов.
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Сапарова Г.А.,
IMMUNOCJRRECTION OF RED FLAT LICHEN OF MUCOUS CAVITY OF MOUTH
Polyoxidonium in complex treatment of patients with red flat lichen of mucous cavity of mouth. contribute to the restoration of local mouth guards, and the overall immune system, accelerates healing and reduces the number of relapses.
Текст научной работы на тему «Иммунокоррегирующая терапия красного плоского лишая слизистой полости рта»
УДК 611.31-616.513.7-616.516 Г.А. Сапарова
Стоматологическая клиника «Ер-стом», г. Семей
ИММУНОКОРРЕГИРУЮЩАЯ ТЕРАПИЯ КРАСНОГО ПЛОСКОГО ЛИШАЯ СЛИЗИСТОЙ ПОЛОСТИ РТА
Полиоксидоний в комплексном лечении больных красным плоским лишаем способствуют восстановлению, как местной защиты полости рта, так и общей системы иммунитета, ускоряет сроки заживления и снижает число рецидивов.
Ключевые слова: красный плоский лишай, полость рта местный и общий иммунитет, иммунокорекция, полиок-сидоний.
Красный плоский лишай остается существенной проблемой современной стоматологии и дерматологии, так как до сих пор не снижается частота заболевания, которое имеет тяжелое хроническое течение, часто торпид-ное к проводимой терапии [1,2]. Частота встречаемости КПЛ за последние 30 лет увеличилась примерно в 2 раза [3,4]. По данным ряда авторов изолированное поражение КПЛ слизистой оболочки рта встречается довольно часто и составляет от 23% до 54% [1,4].
В последние десятилетия ведущую роль в патогенезе КПЛ придается иммуноаллергическим аспектам. Установлено, что в крови больных отмечается снижение числа Т-клеток и их функциональной активности, дисре-гуляция иммунного ответа[4,6,7]. У большинства больных наблюдалось снижение фагоцитарной активности нейтрофилов, как в спонтанном, так и в индуцированном НСТ тесте, что свидетельствовало об истощении резервного потенциала фагоцитов [5]
В настоящее время лечение КПЛ остается сложной задачей. Для терапии данного заболевания применяются лекарственные препараты различных групп, в том числе и иммунотропные препараты. Так, при лечении эрозивно-язвенной формы красного плоского лишая применяли ликопид [8]. и галавит [6]. Учитывая, что по данным литературы и собственных исследований у больных КПЛ выявляются нарушения местного иммунитета и снижение фагоцитарной функции нейтрофи-лов, нами в качестве иммунокорректора использован полиоксидоний. Согласно инструкции полиоксидоний увеличивает резистентность организма в отношении бактериальных, грибковых и вирусных инфекций. Основой механизма иммуномодулирующего действия Поли-оксидония является прямое воздействие на фагоцитирующие клетки и естественные киллеры, а также стимуляция антителообразования. Восстанавливает иммунные реакции при вторичных иммунодефицитных состояниях, вызванных инфекциями, травмами, ожогами, злокачественными новообразованиями, осложнениями после хирургических операций.
При сублингвальном применении Полиоксидоний активирует лимфоидные клетки, находящиеся в бронхах, носовой и ротовой полости, евстахиевых трубах, тем самым повышая устойчивость этих органов к инфекционным агентам.
При пероральном применении Полиоксидоний активирует лимфоидные клетки, находящиеся в кишечнике, а именно В-клетки, продуцирующие секреторные 1дА. Следствием этого является повышение устойчивости ЖКТ и дыхательного тракта к инфекционным агентам. Кроме того, при пероральном применении Полиоксидо-ний активирует тканевые макрофаги, что способствует более быстрой элиминации возбудителя из организма при наличии очага инфекции.
Наряду с иммуномодулирующим действием, Поли-оксидоний обладает выраженной детоксицирующей и антиоксидантной активностью, которые определяются структурой и высокомолекулярной природой препарата. Повышает устойчивость мембран клеток к цитотоксиче-скому действию лекарственных препаратов и химических веществ, снижает их токсичность.
У взрослых и подростков старше 12 лет в комплексной терапии: острых и хронических воспалительных рецидивирующих бактериальных, вирусных и грибковых инфекций ротовой полости, околоносовых пазух, верхних дыхательных путей, внутреннего и среднего уха. [9].
Клиническая апробация Полиоксидония широко представлена при фурункулезе, герпесе, простатите, гнойных инфекциях, при лечении язвенной болезни желудка и у больных раком молочной железы. Основанием при выборе препарата послужило его выраженные рано- и язвозаживляющие свойства, изученные при лечении язвенной болезни желудка и двенадцатиперстной кишки.
В доступной нам литературе мы не нашли работ по изучению клинической эффективности Полиоксидония при лечения КПЛ, что обусловило актуальность работы и послужило предпосылкой для проведения исследования.
Цель исследования: сравнить клиническую эффективность иммунокорректора Полиоксидония у больных КПЛ
Материалы и методы: Всего было обследовано и пролечено в стоматологической клинике «Ер-стом» г. Семей 20 больных с красным плоским лишаем — 15 женщин (75,0%) и 5 мужчин (25,0%), средний возраст составил 60,3 лет.
Все больные были разделены на группы. 1 основная группа — 12 человек, получали в схеме комплексного лечения иммуномодулирующий препарат полиоксидо-ний. Контрольная группа — 8 человек, получали традиционное комплексное лечение, исключающее применение полиоксидония. Контрольные иммунологические исследования проводили в группе 10 здоровых лиц. Пациентам основной и контрольной групп проводилась комплексная терапия: санация полости рта, профессиональная гигиена, устранение травматических факторов и назначение средств общей и местной терапии.
Местное лечение включало назначение традиционных эпителизирующих (солкосерил, актовегин) и обезболивающих средств. Для обезболивания пациентам в контрольных подгруппах назначали аппликации или ротовые ванночки 2% раствора лидокаина. Общее лечение, у пациентов контрольной и основной групп, включало традиционные средства (антигистаминные, витаминные препараты). Пациентам основной группы дополнительно назначали Полиоксидоний в таблетках сублингвально из расчета 12мг -2 раза в день. Курс лечения 15 дней. У пациентов регистрировали показатели
болевой чувствительности элементов поражения до- и в процессе местного лечения и площадь очага эрозивно-язвенного поражения, которую определяли по максимальным вертикальным и горизонтальным размерам.
Для оценки показателей местного иммунитета полости рта и системы фагоцитоза в процессе традиционного лечения и при применении инъекций Полиоксидония изучали динамику изменения содержания в слюне показателя местной иммунной защиты — секреторного иммуноглобулина А и в периферической крови показатели фагоцитоза.
Слюну собирали натощак после ополаскивания полости рта водой путем сплевывания в пробирку объе-
Частота обострений у больных КПЛ.
мом 2 мл, в течение 6 минут, которую затем хранили при 1: — 20°С до момента проведения анализа. Слюну собирали до лечения и в конце лечебного курса. В пробах периферической крови исследовали фагоцитарную систему: фагоцитоз, фагоцитарное число и НСТ тест. Аналогичные исследования проводились в контрольной подгруппе больных, получавших традиционное лечение и здоровых лиц. Все иммунологические исследования проводили в лаборатории Мц ГМУ г.Семей.
Результаты. Длительность КПЛ у пациентов составила от 1 года до 3лет, в течение всего периода заболевания пациенты отмечали периодическое появление болезненных образований в полости рта. (Табл.1)
Группа больных п Обострения
до 3-х раз в год раз в 2-4 месяца постоянное рецидивирование
Опытная 12 4 5 3
Контрольная 8 3 3 2
Контроль за динамикой заживления эрозий у больных показал, что в течение 8-10 дней наблюдения у 5 пациентов основной подгруппы отмечалась полная эпи-тализация эрозий, у 5 — площадь эрозивно-язвенных элементов поражения уменьшилась на половину. В
двух случаях площадь поражения уменьшилась на 10%. У пациентов контрольной подгруппы полная эпитализа-ция выявлена в двух случаях, в 3-х уменьшение площади элементов поражения наполовину и в 3 -х случаях площадь поражения уменьшилась на 10%. (табл.2)
результаты лечения больных КПЛ.
Группа больных п Полная Уменьшение площади Уменьшение площади Рецидивы за
эпитализация поражения на 50% поражения на 10% год
Опытная 12 5 5 2 1
Контрольная 8 2 3 3 3
Анализ клинических наблюдений за год показал, что в первой группе был всего один случай рецидива за год, в то время как во второй было 3 рецидива.
Результаты иммунологических исследований показали, у практически здоровых людей при исследовании слюны выявлены индивидуальные колебания в содержании секреторного иммуноглобулина А (э!дА), По усредненным индивидуальным и групповому показате-
лям содержание данных иммунологических параметров в смешанной слюне составило: в!дА- 103,01±2,55 мкг/ мл. При заболеваниях слизистой оболочки рта показатели секреторного иммуноглобулина А в обеих группах больных были достоверно выше по сравнению со здоровыми людьми (табл.3). У этих больных отмечалось снижение функций фагоцитирующих клеток периферической крови.
Иммунологические показатели у пациентов с КЛШ.
Исследуемые параметры п слюна кровь
в!д А (мкг/ мл) Фагоцитоз (%) Ф.ч НСТ тест
Опытная 12 150,2 ± 2,1* 105,1 ± 2,2** 32,1± 1,2* 39.0± 1,6** 1.5± 0,2* 2.2± 0,2** 4,3± 0,1* 5,8± 0,2**
Контрольная 8 152,1 ± 2,2* 127,3± 2,5** 33,2± 1,3* 35,4± 1,2** 1.4± 0,1* 1,8± 0,1** 4,3± 0,1* 4,8± 0,2**
Норма 10 103,01 ± 2,55 40,0± 2,2 2.2± 0,1 5,8± 0,2
*Показатели до лечения ** Показатели
Содержание секреторного иммуноглобулина А после лечения в 1 группе больных почти соответствовали данным здоровых лиц, а у больных контрольной группы значительно уменьшились, по сравнению с исходными данными, но превышали показатели здоровых. Что касается фагоцитарных показателей, то применение полиоксидо-ния привело к восстановлению функций фагоцитирующих клеток, а в контрольной группе эти показатели были сниженеы по сравнению с данными здоровых лиц.
Таким образом, применение полиоксидония в комплексном лечении у больных КПЛ восстанавливает иммунологические показатели, ускоряет сроки заживления и снижает число рецидивов по сравнению с данными больных получавших только традиционное лечение.
1. Довжанский С.И., Слесаренко Н.А. Красный плоский лишай. Саратов. Издат-во СГУ. — 1990. — С. 176.
2. Евсеева И.К. Особенности клинического течения и лечения некоторых кератозов слизистой оболочки полости рта у лиц пожилого возраста: Автореф. канд. мед. наук. — СПб. — 1997. — 19 с.
3. Машкиллейсон А. Л., Абрамова Е. И., Абудуев Н. К. Клинические особенности эрозивно-язвенной формы красного плоского лишая слизистой рта. // Вестн. дер-матол. —1989. №8. — С. 29-31.
4. Слесаренко Н. А. Красный плоский лишай (современные иммунологические и биохимические аспекты) и методы патогенетической терапии. Автореф. дис.докт. мед.наук. — М. — 1995. — С. 31.
5. Мергембаева Х.С. и др., Клинико-иммунологи-ческие особенности эрозивно-язвенной формы красного плоского лишая слизистой оболочки полости рта // Гигиена, эпидемиология и иммунобиология, — 2010. 4(46). -С.68-71.
6. Цветкова А.А. Иммунокоррегирующая терапия заболеваний слизистой оболочки полости рта. Автореф. канд дисс. — М. 2008, — 17с
7. Рабинович О.Ф., Ханукова A.M., Хамидулнна К.Ф. Особенности иммунного статуса больных с красным плоским лишаем // Стоматология. — 1995. №5. — С. 20-25.
8. Рабинович О.Ф., Рабинович И.М., Пинегин Б.В. Применение иммунокорригирующего препарата «Лико-пид» в комплексном лечении красного плоского лишая слизистой оболочки рта // Институт Стоматологии, -№12, — 2001. -С. 29-34.
АУЫЗ КУЫСЫ ШЫРЫШТЫ КАБАТЫНЬЩ КЫЗЫЛ ЖАЛПАК ТЕМ1РЕТК1С1НЩ ИММУНОКОРРЕГИРЛЕУШ1 ТЕРАПИЯСЫ Г.А. Сапарова Семей к. «Ер-стом» Tic емдеу емханасы
^ызыл жалпак темфетга бар наукастарды кешендi емдеу кезще полиоксидоний ауыз куысыныч жергiлiктi корганысыныщ, сонымен катар иммунитеттщ жалпы жYЙесiнщ калыптасуына, жазылу уакытын жеделдетуге жэне рецидив саныныщ азаюына эсер етедк
Heri3ri сездер: кызыл жалпак темiреткi, ауыз куысы, жергiлiктi жэне жалпы иммунитет, иммунокоррекция, полиоксидоний.
IMMUNOCJRRECTION OF RED FLAT LICHEN OF MUCOUS CAVITY OF MOUTH
G.A. Saparova Dental Clinic «Er-stom» Semey
Polyoxidonium in complex treatment of patients with red flat lichen of mucous cavity of mouth. contribute to the restoration of local mouth guards, and the overall immune system, accelerates healing and reduces the number of relapses.
Key words: red flat lichen, oral cavity, local and General immunity, immunocorrection, polyoxidonium.
УДК 611.31-616.513.7-616.516 Г.А. Сапарова
Стоматологическая клиника «Ер-стом», г. Семей
КЛИНИКО-ИММУНОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ У БОЛЬНЫХ КРАСНЫМ ПЛОСКИМ ЛИШАЕМ
Проведены клинические и иммунологические исследования 20 больных красным плоским лишаем слизистой полости рта. Установлено, что у половины больных отмечалась выраженная болезненность. Отмечено значительное увеличение в слюне секреторного иммуноглобулина А и снижение показателей фагоцитоза, что диктует необходимость проведение иммунокоррекции.
Ключевые слова: красный плоский лишай, слюна, секреторный иммуноглобулина А, система фагоцитоза.
Актуальность. Одним из распространенных заболеваний слизистой оболочки полости рта является красный плоский лишай (КПЛ). Число больных КПЛ имеет тенденцию к постоянному росту, несмотря на современные методы диагностики и лечения заболевания [1].
По данным эпидемиологических исследований КПЛ встречается у 0,1-2% населения, чаще у женщин в возрасте от 40 до 65 лет [2]. В последние годы происходит «омоложение» страдающих этим заболеванием. По-видимому, это связано с нарушением экологии, распространением вирусной инфекции, изменениями реактивности организма и повышенной частотой психоэмоциональных напряжений. Описаны случаи возникновения КПЛ у детей [3]. Изолированное поражение слизистой оболочки полости рта красным плоским лишаем выявляется в 30-35% случаев [4].
Известно, что эрозивно-язвенная и гиперкератотиче-ская формы заболевания являются факультативными предраками с вероятностью онкотрансформации до 7% [1]. По данным многих авторов КПЛ характеризуется полиморфизмом симптомов клинического проявления, тяжелым, длительным, рецидивирующим течением, тор-пидностью к проводимой традиционной терапии [4,6].
В связи с ростом числа пациентов с КПЛ, длительным хроническим течением заболевания, низкими результатами существующих методов лечения данной патологии, возможностью малигнизации процесса актуальным является поиск новых препаратов, обладающих высокой эффективностью и дающих стойкий терапевтический эффект за минимально короткое время. При КПЛ отмечаются выраженные нарушения, как в гуморальном, так и в клеточном звеньях системы иммунитета [5,6,7]. Необходимо применение простых иммунологических методов, позволяющих в повседневной практике оценить иммунологические нарушения и провести их коррекцию.
Цель работы: изучить клинико-иммунологические проявления у больных КПЛ.
Материалы и методы: В стоматологической клинике «Ер-стом» г. Семей было обследовано 20 больных с красным плоским лишаем — 15 женщин (75,0%) и 5 мужчин (25,0%), средний возраст составил 60,3 лет. Контрольную иммунологическую группу составили 10 здоровых лиц.
Показателя местного иммунитета полости рта изучали по содержанию в слюне секреторного иммуноглобулина А и системы фагоцитоза периферической крови.
Современные принципы лечения проявлений красного плоского лишая на слизистой оболочке рта

Дата публикации: 15.06.2018 2018-06-15
Статья просмотрена: 270 раз
Библиографическое описание:
Фазылова Ю. В., Фатихова Р. Р., Блашкова С. Л. Современные принципы лечения проявлений красного плоского лишая на слизистой оболочке рта // Молодой ученый. 2018. №24. С. 289-293. URL https://moluch.ru/archive/210/51445/ (дата обращения: 09.01.2019).
Лечение хронических заболеваний слизистой оболочки рта входит в число наиболее сложных и актуальных проблем в практической стоматологии. Наиболее клинически сложным в диагностике и лечении являются дерматозы с проявлениями, в том числе изолированными на слизистой оболочке — красный плоский лишай. Выбор методов лечения позволяет оптимизировать общие схемы лечения проявлений этого дерматоза на слизистой оболочке рта.
В работе представлены данные, основанные на собственных клинических примерах, об особенностях проявлений красного плоского лишая на слизистой оболочке рта, как осложненных кандидозом, так и без отягощающих факторов.
Ключевые слова: красный плоский лишай, кандидоз полости рта, терапевтическая стоматология, слизистая оболочка рта, поражения слизистой оболочки рта.
Красный плоский лишай (Lichen ruber planus) — хроническое полиэтиологическое заболевание кожи, с проявлениями на слизистой оболочке полости рта. Заболевание выявляется во всех возрастных группах. У 62–67 % женщин старше 40 лет на фоне развития период менопаузы, преимущественно на слизистой оболочке рта. [3,5,8]
Поражение слизистой оболочки рта встречается у 75 % больных с высыпаниями на коже; морфологические проявления могут быть папулезные, экссудативно-гиперемические, буллезные или эрозивно-язвенные. Изолированные поражения слизистой оболочки рта элементами красного плоского лишая колеблется в пределах 25–35 %. [1,3,5,8]
По сей день этиология красного плоского лишая окончательно не выяснена. Существует несколько теорий его возникновения. Мнение большинства авторов в данном вопросе разделяется. Одной из возможных причин является неврогенный фон (нервно-психические потрясения, стрессы, нарушения сна, физические травмы), который тесно связан с эндокринной теорией возникновения КПЛ. Также, большое значение имеют сопутствующие заболевания (сахарный диабет, заболевания желудочно-кишечного тракта, нарушения функций печени), и отягощенный наследственный анамнез. [1,3,5,8]
Красный плоский лишай относится к дерматозам, с проявлением в полости рта. Основным клиническим патоморфологическим элементом является папула, но при экссудативно-гиперемической форме наблюдается эритема застойного типа, при эрозивно-язвенной форме — эритема, эрозия или язва, при буллезной — пузырь, эрозия, эритема, при гиперкератотической — папулы сливаются в бляшки. Элементы поражения чаще всего располагаются на фоне гиперемированной слизистой. Излюбленной локализацией являются слизистая щек по линии смыкания зубов, ретромолярная область, боковые поверхности языка, красная кайма губ. [3,5,8]
Согласно классификации, предложенной Е. В. Боровским и А. Л. Машкиллейсоном (1984), выделены следующие клинические формы красного плоского лишая слизистой оболочки рта: типичная, экссудативно-гиперемическая, эрозивно-язвенная, гиперкератотическая, атипичная, буллезная. [1,2]
Учитывая сложность патогенеза красного плоского лишая, лечение данной патологии вызывает трудности. Получить позитивный результат возможно лишь в случае комплексного и индивидуализированного подхода к пациенту. Основными задачами лечения является ликвидация кератоза, воспаления, нормализация процесса ороговения, а также достижение стойкой ремиссии.
Лечение всех пациентов обязательно начинается с проведения профессиональной гигиены полости рта, обучения рациональной гигиене, санации полоти рта. Под санацией подразумевается устранение местных раздражающих факторов, сошлифовывание острых краев зубов, устранение очагов одонтогенной инфекции.
Рекомендуется консультация врача-ортопеда для оценки состояния имеющихся конструкций.
Лечебный блок, условно говоря, разделяется на 2 этапа:
1 этап — включал в себя проведение инициальной терапии (антисептическая обработка полости рта 0,05 % раствором хлоргексидина биглюконата; аппликационная анестезия гелем лидоксор 10 %, супра- и субгингивальный скейлинг под прикрытием антисептика; введение в пародонтальные карманы препарата «Альвожил» с экспозицией 4–6 часов; назначение общей этиотропной и патогенетической терапии: антибактериальный препарат широкого спектра действия флексид (левофлоксацин) 500 мг 1 раз в день в течение 5 дней; нестероидный противовоспалительный препарат фаспик (L-аргининовая соль ибупрофена) 200 мг 2 раза в день в течение 5 дней, полиферментный препарат вобэнзим 2 таб. 4–5 раз в день в течение 1 месяца; диета, исключающая прием острой, солёной, жареной пищи, а также пищевых продуктов, богатых органическими кислотами:
фрукты (клубника, ананас, клюква, смородина) и овощи (томаты, репа, редька). [5,10]
2 этап — воздействие на очаг поражения КПЛ — включал в себя назначение препарата — производного 4-аминохинолина — плаквенила по 200 мг 2 раза в день в течение не менее 14 дней; комплексного витаминного препарата аевит по 2 капсулы 3 раза в день в течение 1 месяца; антиацидотического средства — раствора димефосфона 15 % по 1 ст. ложке 3 раза день в течении 14 дней. Местная медикаментозная терапия заключалась в использовании антисептических препаратов (раствор хлоргексидина биглюконата 0,05 %), местных противовоспалительных средств (тантум-верде в виде спрея, раствора или таблеток для рассасывания), а также препаратов, стимулирующих регенерацию. [5,10]
Необходимо отметить, что довольно часто КПЛ протекает совместно с кандидозом, которое осложняет основное заболевание. При назначении комплексной терапии нужно учитывать данную особенность, для оптимизации методов лечения.
Кандидоз полости рта — это инфекционное заболевание, которое вызывается грибками рода Candida. Такие дрожжеподобные микроорганизмы являются частью нормальной микрофлоры человека, не оказывая негативного влияния. Однако под воздействием ряда факторов грибок начинает размножаться, вызывая кандидоз. [4,7]
По данным ВОЗ, до 20 % населения мира хотя бы однократно на протяжении жизни перенесли различные формы кандидозной инфекции. Количество больных постоянно растет. Это связано преимущественно с внедрением новых медицинских технологий, созданием новых антибактериальных препаратов, значительным увеличением числа пациентов с иммунодефицитом. [4,6]
Желудочно-кишечный тракт является главным резервуаром инфекции, при этом C.albicans способна колонизировать практически любую часть тракта. При носительстве в ротовой полости первое место занимает C. albicans — 47–75 %, второе — C. tropicalis и C. globrata — 7 %. [4,6,7]
К факторам, которые увеличивают процент носительства кандид, относят: снижение процесса слюноотделения, низкую рН слюны, увеличение концентрации глюкозы в слюне, курение. [4,6,7]
Решающими факторами для возникновения орального кандидоза и патологии, являются: возраст (неонатальный и пожилой); пищевой дефицит; опухоли; ВИЧ-инфекция; химиотерапия; кортикостероиды (гормонотерапия); ношение зубных протезов. [4]
Пациенты предъявляют жалобы на сухость и жжение слизистой оболочки рта. При осмотре определяется творожистый налет белого цвета, легко снимающийся шпателем. Излюбленной локализацией налета является спинка языка, слизистая щек, красная кайма губ, в местах протезного ложа у пациентов, имеющих ортопедические конструкции. [4,7]
Для подтверждения диагноза кандидоз полости рта необходимо провести микробиологическое исследование соскоба с пораженного участка. Для определения кандидоза полости рта наличие колоний должно быть более 1000 КОЕ.
Для лечения кандидоза необходимо назначение антимикотических препаратов, с учетом чувствительности.
Инфицирование Candida albicans может быть важным фактором в злокачественной трансформации КПЛ. В последнее время неуклонно увеличивается заболеваемость кандидозом, при этом наиболее частым возбудителем остается Candida albicans. В исследованиях Лисовской С. А., 2008, показано наличие штаммов, обладающих выраженными дерматонекротическими, адгезивными и гемолитическими свойствами, и отличающихся по ряду биологических свойств от штаммов, выделенных от здоровых лиц. При кандидозе полости рта четко прослеживается влияние неспецифических и иммунологических защитных факторов. Основным специфическим фактором
служит секреторный иммуноглобулин A (S-IgA), вырабатывающийся строго против антигенов гриба. Неспецифические факторы (муцины, гликопротеины слюны, лактоферрин, лизоцим, пероксидаза, белки-статины) вырабатываются постоянно в отношении многих микроорганизмов. Однако активность многих из них существенно снижается в присутствии кандидных протеиназ и, кроме того у C.albicans есть собственные цистатины. [4,6]
Благоприятным для развития кандидоза является и лечение антибактериальными препаратами, приводящее к быстрой смене количественного и качественного состава микрофлоры полости рта. Лишаясь конкурентов и антагонистов, грибы получают возможность адгезии, ускоренного роста и колонизации. Для C.albicans полость рта представляет собой благоприятную среду, кислая среда обеспечивает существование, а при достаточном поступлении углеводов — и быстрое размножение в дрожжевой фазе. Разные типы эпителия, выстилающие поверхность десны, языка, щек и неба, зубы, зубные протезы, требуют активации. [7,9]
Можно сделать вывод, что изучение инфицирования очагов поражения КПЛ слизистой оболочки рта Candina albicans имеет большое диагностическое значение, однако в алгоритме диагностических мероприятий этому аспекту не всегда уделяется должное внимание. Исходя из представленных аналитических данных, не вызывает сомнений, что в этиопатогенезе КПЛ слизистой оболочки рта большое значение имеют эндокринно-обменные и иммунные механизмы. [5,8]
Многие авторы уделяли внимание изучению микробного пейзажа очагов поражения КПЛ слизистой оболочки рта, но не придавалось большого значения инфицированию очагов поражения Candida albicans, которое является одним из факторов риска злокачественной трансформации эрозивно-язвенной формы КПЛ слизистой оболочки рта. [5,8]
На основании изложенного определена цель исследования — оптимизация методов лечения проявлений красного плоского лишая на слизистой оболочке рта.
Материалы и методы исследования.
По данным исследования, проведенного на базе кафедры терапевтической стоматологии ФГБОУ ВО «Казанского государственного медицинского университета» МЗ РФ в период 2017–2018 гг., проанализирована частота, характер поражений, клиническая симптоматика заболевания. Под наблюдением находилось 27 пациентов в возрасте от 47 до 65 лет — женщины, которым по данным анамнеза, клинического осмотра и результатов обследования был диагностирован «красный плоский лишай (КПЛ), типичная, эрозивно-язвенная формы». Локализация патологических элементов преимущественно была на слизистой оболочке щек и боковых поверхностях языка. Для подтверждения диагноза и дифференциальной диагностики все пациентки был обследованы дерматологом, а также консультированы другими специалистами (аллерголог, гастроэнтеролог, эндокринолог и т. д.) в зависимости от соматического статуса обследованных. В качестве дополнительных лабораторных обследований были назначены общий и биохимический анализы крови, анализ крови на парентеральные инфекции и бактериоскопическое исследование соскоба с элементов поражения с целью выявления грибковой контаминации. Для лечения проявлений КПЛ на слизистой оболочке рта всем пациентам проводилась традиционная патогенетическая терапия с назначением препаратов общего и местного действия. Также была проведена профессиональная чистка зубов, подбор средств индивидуальной гигиены — мягкая щетка, зубная паста «Сплат Зеро Баланс». Курс динамического наблюдения составил 4 месяца. Критериями эффективности проводимой терапии явились уменьшение жалоб пациентов, сроки эпителизации эрозивно-язвенных элементов.
Результаты исследования показали, что у 26 (98 %) обследованных наблюдается контаминация слизистой оболочки рта в области поражения дрожжевыми грибами рода Сandida в количестве в среднем 10 3– 10 4 колоний, что осложнило течение красного плоского лишая и определило выраженность клинических симптомов и стойкость к традиционной терапии. В связи этим в состав комплексной терапии КПЛ были включены антимикотики с учетом чувствительности — 15 (57 %) пациенткам был назначен препарат «Пимафуцин» по 1 таблетке (100мг) 4 раза в сутки; остальные пациентки (11 человек) принимали «Нистатин» по схеме: таблетку 500 тыс. единиц помещали за щеку до полного рассасывания после еды и чистки зубов 3 раза в день. Для обработки слизистой оболочки рта с учетом аллергологического статуса 3 раза в день назначался «Тетраборат натрия», разведенный в теплом солевом растворе. Курс лечения составил две недели.
В результате проводимой комплексной терапии проявлений КПЛ на слизистой оболочке, осложненных грибковой инфекцией, нами были диагностированы признаки клинически стойкой ремиссии у 19 (73,2 %) пациенток уже через месяц наблюдения и лечения, что выражалось в отсутствии жалоб и полной эпителизации эрозивно-язвенных элементов КПЛ, уменьшения выраженности сетки Уикхема на фоне хорошей индивидуальной гигиены рта. У 5 (19,2 %) пациенток на этих сроках сохранялись остаточные явления деструктивного поражения КПЛ, а у 2 (7,6 %) пациенток клиническая картина КПЛ не имела достоверных изменений, что возможно связано с нарушениями гигиенического ухода и несоблюдением рекомендаций по лечению в полном объеме. Результаты повторного микологического исследования также показали снижение количества Candida albicans в среднем до 10 колоний, что является вариантом лабораторной нормы.
Обследование в отдаленные сроки — через 4 месяца, показало, что признаки ремиссии КПЛ на фоне отсутствия грибковой контаминации сохранились у 75 % пациентов, находящихся на диспансерном учете.
Вывод: включение в план диагностических мероприятий исследования микробиологического пейзажа с элементов поражения, а в план лечебных мероприятий противомикробных препаратов местного и общего действия у пациентов с проявлениями красного плоского лишая на слизистой оболочке рта, способствует формированию клинически стойкой ремиссии КПЛ уже через месяц от начала лечения, с сохранением полученных результатов на отдаленных сроках наблюдения.
- Гилева О. С., Кошкин С. В., Либик Т. В., Городилова Е. А. и др. Пародонтологические аспекты заболеваний слизистой оболочки полости рта: красный плоский лишай / Пародонтология. — 2017. — № 3 (84). — С.9–14.
- Акмалова Г. М. Концепция патогенетического обоснования комплексного лечения больных с красным плоским лишаем слизистой оболочки рта. Автореферат диссертации доктора медицинских наук / Уфа. — 2016. — 22 с.
- Фазылова Ю. В., Мушарапова С. И. Красный плоский лишай: проявления в полости рта. Современные принципы диагностики и лечения. Учебное пособие. — Казань. — «Конверс». — 2014. — С. 5–12, 40–45.
- Луницина Ю. В., Токмакова С. И. Кандидоз слизистой оболочки полости рта — актуальная проблема стоматологии XXI века / Проблемы стоматологии. — 2012. — № 2. — С. 30–33.
- Леонтьева Е. С. Стоматологические проявления красного плоского лишая и прогностическая значимость факторов, влияющих на его течение. Диссертация на соискание ученой степени кандидата медицинских наук / Казань. — 2014. — С. 52–53, 30–34.
- Сергеев, А. Ю. Кандидоз. Природа инфекции, механизмы агрессии и
- защиты, лабораторная диагностика, клиника и лечение / А. Ю. Сергеев, Ю.
- В. Сергеев. — М.: Триада-Х, 2001. — 472 с.
- Лисовская, С. А. Новый подход к оценке патогенного потенциала
- клинических штаммов Candida albicans: автореф. дис. … канд. биолог.
- наук: 03.00.07 / Лисовская Светлана Анатольевна. — Казань, 2008. — 25 с.
- Заболотный А. И. Красный плоский лишай слизистой оболочки полости рта (клиника, диагностика, лечение) / А. И. Заболотный, Е. Н. Силантьева. — Казань. 2012. — 86 с.
- Рациональная фармакотерапия в стоматологии. Руководство для практических врачей / под ред. Г. М. Барера, Е. В. Зорян. — М.: Литтерра, 2006. — 568 с.
- Литвинов С. Л. Эффективность различных местных медикаментозных препаратов в комплексном лечении больных с красным плоским лишаем слизистой оболочки полости рта / С. Л. Литвинов // Автореферат дисс. канд. мед. наук. — Пермь, 2004. — 137 с.
Лечение плоского лишая в полости рта

Кортикостероидные препараты системного и локального действия занимают ведущее место при лечении многих дерматозов. Широко применяются они и в стоматологической практике [2], особенно при лечении эрозивно-язвенной формы красного плоского лишая слизистой оболочки рта (КПЛ СОР) [1, 3], которая имеет высокий риск онкогенной трансформации (от 1,1 до 7 % случаев) [4], сопровождается значительной болезненностью и торпидностью течения, полиморфизмом клинических проявлений и малой эффективностью лечения. Кортикостероиды обладают противовоспалительным, иммунодепрессивным, гипосенсибилизирующим действием и, таким образом, оказывают разносторонний эффект на иммунопатологические процессы при осложненных формах КПЛ. Наряду с благоприятным терапевтическим действием для глюкокортикостероидов характерны тяжелейшие побочные эффекты, связанные с их влиянием на все виды обмена веществ – белковый, углеводный, жировой и водно-электролитный. В связи с этим препаратом выбора является дипроспан – сильнейший и наиболее безопасный кортикостероид, позволяющий достичь эффекта при небольшом числе инъекций.
Дипроспан обладает высокой глюкокортикостероидной активностью, но, в отличие от своих предшественников (гидрокортизона, преднизолона, кеналога), имеет ряд преимуществ: незначительное минералокортикостероидное действие;
– быстрое и вместе с тем пролонгированное мощное противовоспалительное и
– не вызывает местных мелкокристаллических реакций;
– не оказывает местнодистрофического действия на ткани;
– назначается как однократно, так и повторно (при наличии показаний).
Дипроспан – глюкокортикостероидный препарат, состоит из 2 частей, одна из которых (бетаметазона динатрия фосфат) оказывает немедленное, а вторая (бетаметазона дипропионат) – пролонгированное действие. Препарат выпускается в ампулах по 1 мл, которые содержат 2 мг первого и 5 мг второго вещества.
Бетаметазона динатрия фосфат – легкорастворимый компонент, который быстро всасывается в ткани и обеспечивает быстрый эффект. У бетаметазона дипропроната более медленная абсорбция, благодаря чему создается пролонгированное действие (до 3 недель).
Согласно исследованиям, проведенным фирмой-изготовителем, сравнительный противовоспалительный эффект глюкокортикостероидов (в пересчете на преднизолон) при применении гидрокортизона составляет 0,25, метилпреднизолона и триамцинолона – 1,25, бетаметазона – 6,25. В то же время бетаметазон более безопасен, чем другие глюкокортикостероиды. Индекс безопасности (доза, вызывающая кушингоид/эффективная противовоспалительная доза) для бетаметазона составляет 2,6, для гидрокортизона – 1,3, для метилпреднизолона и триамцинолона – 1,6.
Имеются сведения о применении дипроспана в виде инъекций под элементы поражения слизистой оболочки [1], применяемом в случаях тяжелого упорного течения КПЛ. Авторы указывают на сокращение сроков разрешения и эпителизации эрозивно-язвенных элементов, достижении терапевтической эффективности у 68,0–75,0 % пациентов. Однако осложнением данного метода нередко является грубое рубцевание слизистой в месте инъекций. Ограничения локального инъекционного введения кортикостероидов связано также с его болезненностью.
Целью работы явилась оценка эффективности использования дипроспана при лечении пациентов с эрозивно-язвенной формой КПЛ.
Эффективность применения дипроспана была изучена у 15 больных КПЛ СОР (средний возраст 52 года), которые составили 1-ю группу: получали внутримышечно по 1 мл дипроспана 1 раз в месяц (рис. 1). 11 пациентов (средний возраст 52 года) с эрозивно-язвенной формой составили контрольную группу. Во всех случаях лечение было комплексным и включало санацию полости рта, рациональное протезирование (замена некачественных и изготовленных из разнородных металлов ортопедических конструкций). С целью обследования и лечения сопутствующей патологии больных направляли к соответствующим специалистам, чаще всего, это терапевты, гастроэнтерологи, кардиологи, эндокринологи или клинические иммунологи.
Общая терапия для всех пациентов включала в себя назначение внутрь седативных средств – атаракса по 0,25 мг 1 раз в день, комплекса витаминов: витрум или супрадин – по 1 таблетке в день в течение 1 месяца, иммуномодулирующего препарата ликопид 10 мг 1 раз в день в течение 10 дней, антигистаминного препарата цетрин – по 1 таблетке ежедневно в течение 14 дней.
Местная терапия включала при необходимости – обезболивание СОР 5 % анестезиновой эмульсией, антисептическую обработку 0,2 % раствором хлоргексидина, аппликации ферментов (трипсина), смазывание пораженных участков холисал-гелью. Затем в обеих группах использовали аппликации кератопластического средства – солкосерил адгезивной пасты.
Эффективность проводимой терапии оценивали в динамике на 7, 14, 21-й дни лечения, а также через 1,5 и 2,5 месяца после лечения по следующим параметрам:
А. Уменьшение или исчезновение субъективных ощущений в полости рта (болевой синдром, жжение) по визуально-аналоговой шкале боли (VAS). Для этого при каждом посещении больным предлагалось оценить в баллах наличие спонтанной и возникающей при приеме пищи боли в СОР в диапазоне от 0 (нет боли) до 4 (сильные боли) [5].
Б. Сокращение размеров или исчезновение очагов поражения по клинической оценке для измерения очагов поражения [6].
0 – нет поражения, 1 – наличие белых папул без воспаления, 2 – папулы с гиперемией на СОР, 3 – гиперкератоз с эрозивными участками менее чем 1 см, 4 – гиперкератоз с эрозивной площадью более 1 см, 5 – гиперкератоз с эрозивной площадью более 1 см и язвенным поражением.
Результаты данных обработаны стандартными методами вариационной статистики, с использованием программных пакетов статистической обработки Statistica 6.0 for Windows. Оценку достоверности различий (р) между группами определяли с помощью критерия Стьюдента (t).
Результаты исследования и их обсуждение
Через 7–10 дней после первой инъекции прекращалось появление новых элементов, за несколько дней до этого исчезала боль, на 21-й день лечения значение симптома боли у всех больных в основной группе оставалось низким и составило 1,12 ± 0,57 баллов, что в 2,1 раза меньше, чем в группе сравнения, где VAS составила 2,34 ± 0,54 балла, где у 59 % больных до конца лечения сохранялись жжение, чувство стянутости, иногда боль при приеме пищи.
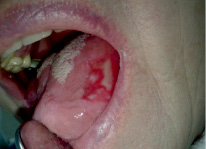
Рис. 1. Пациентка Ш. Эрозивно-язвенная форма КПЛ, до лечения
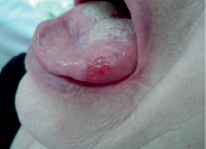
Рис. 2. Пациентка Ш., после лечения
На 14-й день лечения отмечали достоверное уменьшение площади эрозий у всех пациентов основной группы, а в группе сравнения те же изменения наблюдались только у 4 пациентов, что в 3,8 раза меньше, чем в основной группе (р
Лечение плоского лишая в полости рта

В настоящее время этиология и патогенез красного плоского лишая слизистой оболочки полости рта (КПЛ СОПР) остаются малоизученными, а лечение заболевания представляет определенные трудности [2, 6, 7, 9]. Согласно данным последних публикаций отечественных и зарубежных авторов, КПЛ принято рассматривать как мультифакторное заболевание, в патогенезе которого участвуют различные нейроэндокринные, иммунные, интоксикационные и метаболические процессы [3, 7, 9].
Клиническая картина и морфология КПЛ СОПР не достаточно изучены [1, 2, 4, 8]. Клинические проявления КПЛ СОПР, подтвержденные патогистологическими исследованиями, позволяют диагностировать данное заболевание. Сочетание ряда патогистологических признаков делают морфологическую картину процесса КПЛ СОПР довольно определенной: патологическое присутствие зернистого слоя, паракератоз, гиперкератоз, акантоз. В то же время результаты многих исследований свидетельствуют о многообразии морфологических изменений, развивающихся в СОПР при КПЛ [2, 3, 5, 10]. В связи с изложенным представляется целесообразным более детальное изучение морфологической картины КПЛ СОПР, так как это позволит в дальнейшем оценить результаты и эффективность проводимого лечения.
Цель исследования: изучить патоморфологические особенности КПЛ СОПР при разных клинических формах заболевания.
Материал и методы исследования
Проведено клиническое стоматологическое обследование 66 больных с типичной и эрозивно-язвенной формами КПЛ СОПР в возрасте от 35 до 65 лет (средний возраст — 54,3 ± 1,3 лет), из них 18 мужчин и 48 женщин. Исследование проведено с соблюдением принципов добровольности и конфиденциальности в соответствии с «Основами законодательства РФ об охране здоровья граждан» (Указ Президента РФ от 24.12.1993 № 2288). Обследование пациентов и использование полученных данных в научных исследованиях проводили после разрешения Локального комитета по медицинской этике.
Патоморфологическое исследование биоптатов очагов поражения слизистой оболочки щеки выполнено у 23 больных (10 мужчин и 13 женщин — 43,5 и 56,5 % соответственно) КПЛ СОПР с типичной (n = 12) и эрозивно-язвенной (n = 11) клиническими формами. Длительность заболевания составила в среднем 1,8 ± 0,4 года. Биоптаты исследовали до и после включения в комплексную терапию больных иммуномодулятора. В качестве иммуномодулятора пациентам дополнительно назначали «Неовир» (оксодигидроакридинилацетат натрия), относящийся к группе низкомолекулярных синтетических индукторов интерферона (Фармавит, С.-Петербург). Контрольная группа состояла из 15 практически здоровых лиц, без воспалительных поражений СОПР: 8 (53,3 %) мужчин и 7 (46,7 %) женщин.
Исследовали биоптаты СОПР размерами 2,0×2,0 мм, взятые со слизистой оболочки щеки. У больных КПЛ иссечение фрагментов слизистой оболочки щеки производилось из очагов поражения вблизи границы здоровой ткани. Процедуру биопсии осуществляли под местной анестезией (2 %-й раствор лидокаина). В качестве «здорового контроля» использовали биоптаты пациентов без патоморфологических признаков в СОПР.
Для патогистологического исследования ткань фиксировали в течение суток в 10 %-м растворе нейтрального формалина на фосфатном буфере pH 7,5. Парафиновые срезы, заключенные в гистовакс, окрашивали гематоксилином и эозином с постановкой реакции Перлса и по ван Гизону. Исследование и морфометрический анализ проводили в универсальном микроскопе Leica DM 4000B с использованием цифровой фотокамеры Leica DFC 320 и компьютерной программы Leica QWin.
Статистическую обработку результатов осуществляли с вычислением среднего значения, ошибки среднего. Значимость различий определяли по критерию Стьюдента. Различия считали статистически достоверными, если достигнутый уровень значимости (р) не превышал принятого критического уровня значимости, равного 0,05.
Результаты исследования и их обсуждение
Наиболее часто КПЛ СОПР встречался у больных в возрасте 50-59 лет (51,5 % случаев). Средний возраст пациентов с типичной формой заболевания составлял 50,1 ± 1,4 лет, эрозивно-язвенной формой —
58,8 ± 1,5 лет (на 8,7 лет превышал средний возраст больных с типичной формой). Количество женщин в группах исследования преобладало над количеством мужчин в 2,6 раза. Среди больных с типичной формой КПЛ СОПР женщин было в 3,5 раза больше, чем мужчин, а среди пациентов с эрозивно-язвенной формой — в 3,7 раза. Длительность заболевания составила от 3 мес. до 9 лет (в среднем 2,2 ± 0,5 года). Средняя длительность заболевания при эрозивно-язвенной форме (3,0 ± 0,9 года) была в 2 раза выше, чем при типичной форме (1,5 ± 0,3 года).
Среди факторов, провоцирующих начало или обострение заболевания, 21,2 % больных отмечали стрессовые ситуации, 18,1 % — пищевые раздражители, 16,6 % — протезирование съемными и несъемными конструкциями, 12,1 % — механическую травму, 6,1 % — аллергические состояния, 4,5 % — прием лекарственных препаратов. У 7,5 % пациентов КПЛ СОПР развивался вскоре после инфекционных заболеваний, а 13,6 % больных не смогли указать ни на один из провоцирующих факторов. У 87,8 % больных КПЛ СОПР сочетался с заболеваниями желудочно-кишечного тракта и в 63,6 % случаев — с функциональными нарушениями нервной системы.
Наиболее часто КПЛ локализовался на слизистой оболочке щек — 87,8 % больных; у 36,3 и 28,7 % больных отмечали локализацию соответственно в ретромолярном пространстве и на слизистой оболочке спинки и боковых поверхностей языка. Слизистая оболочка твердого и мягкого неба, губ и дно полости рта поражались значительно реже (соответственно в 7,5; 10,6 и 4,5 % случаев).
У всех обследованных больных КПЛ СОПР выявлены изменения в составе микрофлоры полости рта. Анализ результатов исследования показал, что отклонения в составе и свойствах микрофлоры были разными у больных с типичной и эрозивно-язвенной формами КПЛ СОПР. Наиболее выраженные изменения микрофлоры полости рта отмечены у больных с эрозивно-язвенной формой КПЛ СОПР. Так, при типичной форме изменения микрофлоры полости рта в большинстве случаев (81,2 %) диагностированы как дисбиотический сдвиг и дисбактериоз I-II степени в отличие от эрозивно-язвенной формы заболевания, при которой в 79,4 % случаев выявлен дисбактериоз III-IV степени. Кандидозная инфекция выявлена у всех больных с дисбактериозами слизистой оболочки полости рта, что соответствовало дисбиотическому сдвигу и I-II, III и IV степени дисбактериоза. При дисбиотическом сдвиге клинических проявлений кандидоза не наблюдалось.
Структурные изменения слизистой оболочки щеки у больных КПЛ СОПР зависели от формы воспалительного процесса (типичной или эрозивно-язвенной) и были наиболее выраженными при эрозивно-язвенной форме заболевания. Наиболее частыми патоморфологическими признаками в исследуемом материале больных КПЛ СОПР были утолщение эпителиального слоя слизистой оболочки щеки за счет пролиферации базальных и шиповидных клеток (акантоз), иногда акантоз с типичным для КПЛ заострением эпителиальных межсосочковых отростков книзу (симптом пилы), чрезмерное увеличение поверхностного слоя (гиперкератоз) с участками сохранения ядер в поверхностных клетках шиповидного слоя (паракератоз). Выявлялось также утолщение зернистого слоя (гранулез). В сосочковом слое СОПР наблюдался диффузный полосовидный лимфоидный инфильтрат.
В некоторых случаях граница между эпителием и субэпителиальным слоем была «размытой» клетками инфильтрата. Ороговение слизистой оболочки в зоне папул выявлялось у 78 % больных КПЛ СОПР. В основном у этих больных гипер- и паракератоз сочетались с явлениями акантоза. Количество клеток в шиповатом и базальном слоях эпителия, а также количество слоев клеток были увеличенными. До лечения паракератоз в той или иной степени отмечался у 29 % больных. При этом зернистый слой не был выраженным. Эти признаки можно рассматривать как нарушение процессов дифференцировки эпителиоцитов.
В биоптатах СОПР большинства больных до лечения отмечалось наличие воспалительноклеточной инфильтрации. Клеточный инфильтрат локализовался в основном вокруг сосудов микроциркуляторного русла (преимущественно венул и капилляров). Реже инфильтрат располагался вне связи с сосудами. Инфильтрат был представлен в основном лимфоцитами с примесью небольшого числа макрофагов и единичными гранулоцитами (в основном нейтрофилами); встречались единичные эозинофилы. Воспалительно-клеточный инфильтрат располагался преимущественно в верхней части собственно пластинки. У 11 % больных интенсивность клеточной инфильтрации мы расценили как выраженную, в преобладающем числе она была умеренной, в 23 % случаев она практически отсутствовала. Сочетание патогистологических признаков, описанных выше, отмечалось у подавляющего большинства больных.
Типичной форме КПЛ СОПР соответствовали классические морфологические признаки заболевания: акантоз, гиперкератоз, паракератоз, гранулез, размытие границ базального слоя инфильтрата, состоящего преимущественно из лимфоцитов. При эрозивно-язвенной форме КПЛ СОПР гистологическая картина характеризовалась такими же изменениями, как и при типичной форме, за исключением резко выраженного отека, расширений сосудов стромы; регистрировались дефекты эпителия. Шиповатый и базальный слои эпителия были утолщенными за счет активации пролиферативных процессов, отростки эпителия при этом удлинялись.
Комплексная терапия больных КПЛ СОПР с применением противовоспалительного иммуномодулирующего препарата «Неовир» оказала положительное влияние на клинико-лабораторные показатели. В динамике и на момент окончания лечения происходило более быстрое по сравнению с группой больных, не получавших препарат, сокращение площади папулезных элементов, размеров эрозий, отека, гиперемии в очаге поражения, купирование болевого синдрома и жжения в СОПР, отмечалась более длительная клиническая ремиссия.
При включении в комплексную терапию иммуномодулятора «Неовир», обладающего противогрибковой и антибактериальной активностью, происходила нормализация микробиоценоза у всех пациентов с типичной формой КПЛ СОПР и у большинства пациентов с эрозивно-язвенной формой.
В результате комплексной терапии с использованием «Неовира» при сочетании с противогрибковыми препаратами у пациентов с типичной и эрозивно-язвенной формами КПЛ наблюдалась тенденция к нормализации микробной флоры полости рта соответственно к 14-18 и 28-30 дню. При проведении традиционной терапии тенденция к улучшению микрофлоры у больных с типичной и эрозивно-язвенной формами КПЛ отмечалась только после повторного курса лечения.
Сравнительное исследование биоптатов СОПР у одних и тех же больных, взятых до и после традиционной терапии с использованием иммуномодулятора, выявило положительную динамику морфологических изменений. Это, прежде всего, касалось количества и размеров инфильтратов в собственной пластинке. Инфильтрация сохранялась в основном вокруг мелких сосудов. Явления акантоза, гипер- и паракератоза также подверглись существенной регрессии. На фоне иммуномодулирующей терапии индекс пролиферации (по экспрессии Ki-67) значительно снижался и составлял 22,1 ± 1,1 %, что было в 2 раза ниже, чем до лечения (45,0 ± 1,0 %, р
