Иванов экзема
Инфекционная экзема и атопический дерматит: комплексный подход к лечению
Этиопатогенез
Рост заболеваемости, недостаточная ясность патогенетических звеньев, хроническое рецидивирующее течение, патоморфоз клинической картины экземы и АД, нередко — развитие осложненных форм, которые приводят к временной или стойкой утрате трудоспособности, рефрактерность к стандартной терапии и негативное влияние на качество жизни больных обусловливают заинтересованность данной проблемой ученых.
Мультифакторный этиопатогенез экземы и АД свидетельствует о комплексном характере нарушений со стороны многих систем организма пациентов. В последние годы повышенное внимание было уделено изучению состояния иммунной системы у таких больных.
Актуальным и целесообразным является дальнейшее изучение патогенетических механизмов дерматозов, что будет способствовать улучшению качества жизни пациентов за счет применения соответствующих средств терапевтической коррекции (подробнее можно узнать здесь).
Комплексный подход к терапии
Современная врачебная тактика при лечении больных инфекционной (микробной) экземой (ИЭ) и АД, как правило, имеет патогенетическую и симптоматическую направленность. Комплексная терапия данных дерматозов включает проведение следующих мероприятий:
- гипоаллергенный рацион;
- лечение медпрепаратами;
- физиолечение;
- курортное лечение;
- предупреждающие меры.
При традиционном лечении медпрепаратами больные ИЭ и АД получают антигистаминные, десенсибилизирующие, седативные, ферментные, витаминные средства, а также наружную терапию. В то же время до сих пор учеными ведется поиск эффективных методов лечения этих дерматозов.
Многочисленные исследования иммунокоррекции при ИЭ и АД показали эффективность препаратов, направленных на стимуляцию Т-клеточного звена иммунитета, факторов неспецифической резистентности организма, нормализации уровня IgА, IgМ , IgG, IgЕ и ускорения элиминации циркулирующих иммунных комплексов (ЦИК).
Однако эти препараты не всегда достаточно эффективны, о чем свидетельствует высокий уровень рецидивирования указанных дерматозов, который сохраняется и сейчас. Все это создает необходимость поиска новых иммуномодулирующих препаратов для использования в комплексной терапии ИЭ и АД.
Перспективными оказались данные об иммуномодулирующем действии Протефлазида — растительного флавоноидного препарата с присущим ему интерфероногенным и противовирусным действием, апоптозомодулирующей и антиоксидантной активностью, что способствует повышению неспецифической резистентности и общего уровня иммунного статуса организма.
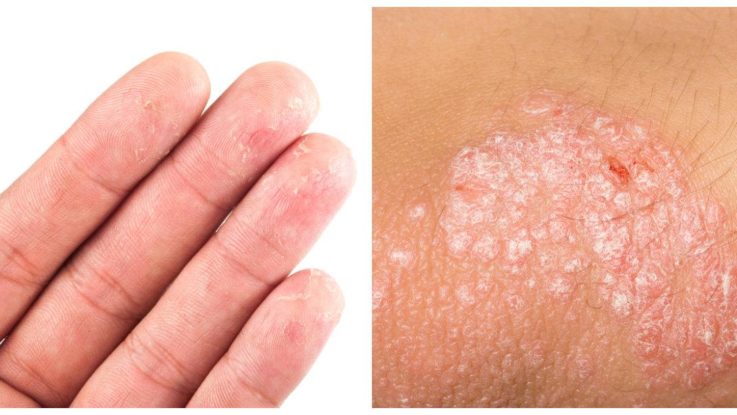
Наибольшее количество больных ИЭ имеют давность заболевания от 10 до 20 лет с отягощенным семейным анамнезом, меньшую часть составляют пациенты с длительностью заболевания до 1 года, частота обострений — 1-2 раза в год. У всех больных АД заболевание начинается с первых лет жизни, при этом его продолжительность составляет 18-65 лет, частота обострений колеблется от 2 до 5 раз в год.
При ИЭ в основном болеют мужчины старше 40 лет и имеют характерный клинический полиморфизм (отек, эритема, везикула – у 100% больных, «экзематозные колодцы», корки – 99%, зуд – 98%, инфильтрации, экскориации – 88%, шелушение, лихенификация – 85%). У больных ИЭ развивается на месте очагов (хронических) инфекции, чаще начинаясь как несимметричный процесс на коже голеней, тыле кистей, волосистой части головы.
Среди больных ИЭ выявляется превалирование микотической природы поражения кожи, преобладание распространенных форм и средней степени тяжести. Характерные внесезонные обострения — у 53% больных.
При АД чаще болеют женщины в возрасте от 18 до 29 лет. Клинически процесс характеризуется преобладанием признаков хронического процесса: папулезных высыпаний (100%), шелушение (91%), инфильтрации (94%), развитие у большей части больных стабильных признаков дерматоза – сухости (79%), дисхромии, фолликулярного гиперкератоза (69%).
Кожные высыпания у больных локализуются преимущественно на разгибательных поверхностях рук-ног, передне-задней и боковой поверхности шеи, локтевых и подколенных ямках, тыле кистей. Всех больных мучает зуд разной интенсивности.
Характерно преобладание больных с эритематозно-сквамозной формой с лихенификацией; большая часть имеет распространенный характер поражения. Отмечается присоединение повторной инфекции (микозы – у 46%, пиодермии – 30%); у пациентов с локализованными формами дерматоза старших возрастных категорий характерно длительное рецидивирующее течение, сокращение сроков ремиссии, потеря сезонности заболевания.
Диагностика
Клинический диагноз ИЭ и АД устанавливают на основании жалоб больных, анамнеза жизни и заболевания, результатов физикального обследования, а также данных лабораторных методик. Общеклиническое обследование всех больных включает всеобщий анализ крови, всеобщий анализ мочи, копрограмму, биохимический анализ крови, иммунограмму, комплекс серологических реакций (КСР), ЭКГ, при необходимости — консультации смежных специалистов.
Тяжесть течения АД у больных определяют по шкале SCORAD, разработанной Европейской рабочей программой, учитывая распространенность кожного процесса, интенсивность клинических проявлений и субъективные симптомы.
Иммунологическое обследование охватывает количественную оценку основных популяций и субпопуляций лимфоцитов методом иммунофенотипирования с использованием панели ФИТЦ-меченых моноклональных антител.
Анализ показателей клеточного и гуморального звеньев иммунной системы, неспецифической защиты организма у больных ИЭ обычно выявляет значительные нарушения, которые имеют разнонаправленный характер, зависят от степени тяжести заболевания, играют патогенетическую роль в возникновении и прогрессировании данной патологии.
У больных АД обнаруживается дисбаланс Т-звена иммунитета: снижение абсолютного и относительного содержания СD3 клеток. Выявляемые различия в нарушениях отдельных показателей системы иммунитета обусловлены клинической формой и тяжестью течения АД.
Лечение больных осуществляется по принципу индивидуальной патогенетической терапии. Для нормализации дезадаптационных нарушений системы иммунитета в комплекс лечения на фоне вышеупомянутой традиционной терапии больных ИЭ и АД включают Протефлазид (иммунокорригирующий препарат растительного происхождения, полученный из диких злаковых растений Deschampsia caespitosa L. и Calamagrostis epigeios L.).
Использование метода индивидуализированной патогенетической терапии (с учетом особенностей клинического течения и иммунологических нарушений пациентов) с включением препарата Протефлазид на фоне традиционного лечения позволяет значительно повысить эффективность терапии пациентов с ИЭ и АД: ускорение регресса клинических проявлений заболевания, сокращение сроков лечения, уменьшение числа рецидивов и увеличение продолжительности ремиссии.
Клеточный и гуморальный иммунитет, а также факторы неспецифической защиты имеют тенденцию к нормализации, достигая показателей здоровых лиц.
Экзема: причины возникновения


Возникновение экземы – результат воздействия множества факторов. К ней могут привести различные болезни, постоянное влияние окружающей среды (температура, влажность воздуха), а также ряд раздражителей. Кроме того, сегодня медицина выделяет и профессиональную экзему, причины появления которой заключаются в особенностях внутреннего микроклимата некоторых производств.
Экзема – это кожное заболевание, характеризующееся такими симптомами, как воспаление кожных покровов, высыпания на разных частях тела. Выделяют три вида болезни: острую, подострую и хроническую экземы.
Причины появления экземы, как правило, связывают с действием одного или группы факторов:
- Наследственность.
- Снижение иммунитета. Его причина чаще всего кроется в недостатке витаминов.
- Гормональные расстройства.
- Заболевания желудка и печени.
- Несоблюдение личной гигиены. Закупоривание пор кожи приводит к воспалениям, появлению угрей.
- Стрессы, постоянное нервное напряжение. Эта причина может привести не только к возникновению экземы, но и к обострению уже существующего кожного заболевания.
Кроме этого, часто болезнь встречается у работников металлургических, химических, фармацевтических и пищевых производственных предприятий. Реакция на разные вещества развивается постепенно, а потом приобретает стойкий характер.
Детская экзема, как правило, развивается вследствие диатеза и дерматита. Поэтому профилактика у детей заключается в здоровом питании и правильном устранении аллергических реакций.
Факторы, которые предрасполагают к болезни
Описанные выше причины заболевания сами являются следствием разных нарушений в организме. Поэтому мы составили список проблем, которые помогут понять, от чего появляется экзема:
- Избыток витамина В6 в организме.
- Недостаток микроэлементов и ненасыщенных жирных кислот. Приводит к ослаблению иммунной системы, расстройствам желудка.
- Глистные заболевания. Нарушают внутреннюю микрофлору, ведут к дефициту различных витаминов и микроэлементов в организме, нарушению пищеварительных процессов.
- Воспаление желчного пузыря.
Профилактика возникновения экземы
Существует несколько правил, которые помогут сократить риск появления данной болезни:
- Соблюдать личную гигиену тела, принимать душ минимум 1 раз в день.
- Вести здоровый образ жизни.
- Правильно питаться, включать в свой рацион больше витаминов.
- Избегать стрессов и переутомления.
Автореферат и диссертация по медицине (14.01.10) на тему: Совершенствование комплексной терапии микробной экземы


Автореферат диссертации по медицине на тему Совершенствование комплексной терапии микробной экземы
На правах рукописи
Никонова Ирина Владимировна
Совершенствование комплексной терапии микробной экземы.
14.00.11. — кожные и венерические болезни
Автореферат диссертации на соискание ученой степени кандидата медицинских наук
Работа выполнена в Государственном бюджетном образовательном учреждении высшего профессионального образования «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации.
доктор медицинских наук, профессор
доктор медицинских наук, профессор кафедры кожных и венерических болезней лечебного факультета ГБОУ ВПО РНИМУ имени Н.И. Пирогов а Минздрава России
доктор медицинских наук, профессор кафедры кожных и венерических болезней лечебного факультета ГБОУ ВПО 1 МГМУ имени И.М. Сеченова Минздрава России
Орлов Евгений Владимирович
Пашинян Альбина Гургеновна
Ломоносов Константин Михайлович
Российский университет дружбы народов Министерства образования Российской Федерации
Защита состоится «_»__2013 года в 14.00 часов на заседании
диссертационного совета Д 208.072.10 на базе ГБОУ ВПО РНИМУ имени Н.И. Пирогова Министерства здравоохранения Российской Федерации по адресу: 117997 г. Москва, ул. Островитянова, д. 1.
С диссертацией можно ознакомиться в научной библиотеке ГБОУ ВПО РНИМУ имени Н.И. Пирогова Министерства здравоохранения Российской Федерации по адресу: 117997 г. Москва, ул. Островитянова, д. 1.
Автореферат разослан «_»_2012 года
Ученый секретарь диссертационного совета доктор медицинских наук, профессор
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Экзема в структуре дерматологической заболеваемости составляет от 18 до 40%, а среди разнообразия клинических форм заболевания микробная экзема встречается у 12 — 27% (Оркин В.Ф., Олехнович Н.М., 2002; Легессе Д.Г.. 2004; Маркова О.Н., 2006; Judge М„ 2005).
Утрата временной трудоспособности при экземе достигает 36% от всех трудопотерь при дерматозах В структуре госпитализированных на долю больных экземой приходится более 30% (Муниева С.Х., 2006).
Экзема распространена во всех климатогеографических зонах мира. За последние 20 лет отмечается практически десятикратное увеличение распространенности экземы в мире вообще. Примерно один из пяти европейцев страдает от этого хронического воспалительного заболевания кожи.(Кочергин Н.Г., 2003).
Важность, изучаемой проблемы определяется не только ростом заболеваемости; но и особенностями современного течения микробиой экземы, которая имеет тенденцию к более тяжелому течению; сопровождается, частыми продолжительными рецидивами, значительным распространением патологического процесса на коже, а также характеризуется резистентностью к стандартным методам лечения (Дегтяр Ю.С., 2005; Vartianen Е. etal., 2002).Наличие у больных экземой иммунодефицита по клеточному и гуморальному звеньям способствует формированию очагов хронической инфекции и персистенции на коже преимущественно патогенных микроорганизмов (Соколова Т.В., 2007; McFadden L.P., 2000).
Нередко очаги микробной экземы формируются на фоне варикозного симптомокомплекса, длительно незаживающих травм, послеоперационных ран, трофических язв (Савельева B.C., 2000; Кирилюк И.А., с соавт., 2005). Это способствует значительному нарушению барьерной функции кожи. Воздействие микробного фактора (пиококки, грибковая инфекция) на фоне иммунодефицита приводит к персистенции микробных аллергенов, сенсибилизации организма к инфекционному агенту и белковым компонентам собственной кожи (аутосенсибилизации) (Олехнович Н.М., 2001;Кунгуров Н.В. с соавт.. 2005).
Таким образом, терапия микробной экземы является весьма актуальной проблемой клинической медицины.
Существующие методы исследования не всегда позволяют прогнозировать течение экземы (Мавлянова Ш.З., 2001; Маркова О.Н., 2006).
В этой связи, важным аспектом представляется выработка комплексного подхода к различным методикам лечения данного заболевания с учетом современных достижений медицинской науки, в том числе клинической иммунологии. С целью уточнения представления о механизмах развития микробной экземы, пополнения диагностических возможностей, необходимо расширение спектра исследуемых показателей иммунного статуса. Актуальным является направление, посвященное изучению состояния цитокинового статуса при микробной экземе.
В настоящее время перспективным направлением в лечении хронических дерматозов, в частности экземы, является использование немедикаментозных методов. Это обусловлено нарастающей аллергизацией населения, увеличением антибиотикорезистентной кожной микрофлоры, наличием противопоказаний и побочных эффектов при назначении лекарственных препаратов, увеличением количества сопутствующих заболеваний у пациентов, а также высокими ценами на лекарственные препараты (Кошелева И.В., и соавт.,2003). В литературе имеются сведения об успешном клиническом использовании немедикаментозных, нетрадиционных методов лечения экземы (Корсун В.Ф., Кубанова A.A., 1995;Иванов О.Л., 1997; Кошелева И.В., Иванов О.Л., 2003; Якушкина Н.Ю., Силина Л.В., 2005). С учетом механизма действия лазерного излучения на организм разработаны дерматологические показания к лазеротерапии (Москвин C.B., 2003). Однако, в литературе отсутствуют сведения о комбинированном воздействии низкоинтенсивного излучения лазера и распыленного жидкого лекарственного препарата при лечении микробной экземы.
Цель работы — Оценить эффективность применения низкоинтенсивного лазерного излучения в сочетании с распыленными жидкими лекарственными препаратами на очаги микробной экземы.
1. Определить микробиологический спектр и иммунологические показатели у больных микробной экземой.
2.Разработать алгоритм оценки реакций организма пациентов и прогнозирования течения микробной экземы на основе проведенных иммунологических исследований.
3. Оценить терапевтическую эффективность применения еочетанной лазерной терапии у больных микробной экземой с учетом клинической картины.
4. Провести сравнительный анализ результатов лечения больных микробной экземой, получавших общепринятое лечение и пациентов, получавших лазеротерапию в комплексном лечении.
Дополнено представление об иммунопатогенезе воспаления при микробной экземе. Отмечено, что изменение уровня провоспалительных цитокинов отражает неполноценность клеточного иммунного ответа.
Предложен способ прогнозирования течения и развития распространенной микробной экземы на основе определения иммунологических показателей крови.
Разработан способ лазеротерапии больных с микробной экземой, сочетающий воздействие лазерного излучения и накопления лекарственного препарата в патологическом очаге.
Получены доказательства об эффективности комплексного лечения больных с использованием лазеротерапии.
Разработан высокоэффективный комбинированный метод лечения больных микробной экземой аппаратом Комбис-1 с использованием лазерного излучения и наружного мелкодисперсного распыления антибактериальных лекарственных средств. Внедрение предлагаемого метода обеспечивает сокращение сроков пребывания больных в стационаре и удлиняет период ремиссии дерматоза, показывая высокую клиническую эффективность лечения.
Определение гуморальных и клеточных факторов иммунитета, уровней провоспалительных цитокинов позволяет достоверно оценить динамику патологического процесса в коже и предупредить развитие осложнений.
Предложенная классификация иммунологических нарушений при микробной экземе и разработанная математическая модель дополняют имевшиеся ранее представления об иммунопатологических изменениях не только при воспалительном процессе в коже, но и в организме в целом.
Полученные данные могут быть использованы в практической работе дерматологических клиник и отделений.
Основные положения, выносимые на защиту.
1. Среди разновидностей микробной экземы наиболее часто встречаются распространенные формы с подострым и хронически-рецидивирующим течением.
2. Развитие микробной экземы в большинстве случаев обусловлено ассоциацией стрептококка со стафилококком или с грамотрицательной флорой.
3. У пациентов с микробной экземой, выявлены изменения в показателях клеточных, гуморальных факторов иммунитета и цитокинового статуса. Уровни CD8+,CD16+,CD25+,CD95+,HLA-DR+ клеток, концентрации IgA. ИЛ-la, ИЛ-Iß, ИЛ-8, ФНО-a и ИНФ-у, а также индекс CD4+/CD8+, ФАЛ и СН50 являются наиболее значимыми при прогнозировании варианта развития микробной экземы.
4. Использование аппарата Комбис-I в комплексном лечении больных микробной экземой значительно повысило эффективность терапии.
Основные положения диссертации доложены и обсуждались на заседаниях Самарского отделения Всероссийского научного общества дерматовенерологов (Самара, 2009, 2010); на научно-практической конференции «Актуальные проблемы дерматовенерологии» (Самара, 2009); на III Всероссийском конгрессе дерматологов (Казань, 2009); на IV Междисциплинарной научно-практической конференции «Современные методы диагностики, лечения кожных болезней и инфекций, передаваемых половым путем» (Казань, 2011); на конференции молодых исследователей ГБОУ ВПО СамГМУ Росздрава «Аспирантские чтения» (Самара, 2011).
Разработанные практические рекомендации применяются в условиях отделений дерматовенерологии и госпитальной хирургии клиник ГБОУ ВПО СамГМУ Росздрава. Материалы диссертации используются в процессе преподавания студентам и врачам на курсе последипломной подготовки на кафедрах кожных и венерических болезней; госпитальной хирургии ГБОУ ВПО СамГМУ Росздрава.
По теме диссертации опубликовано 5 научных работ, в том числе 2 в журналах, рекомендуемых ВАК Минобрнауки РФ.
Личный вклад автора
Автором подготовлен обзор данных отечественных и зарубежных источников литературы по теме исследования. Проведено углубленное клинико-анамнестическое обследование больных, включая изучение анамнеза, анализ продолжительности заболевания, провоцирующих факторов, сопутствующих заболеваний, качества жизни пациентов, предшествовавшей терапии, а также тяжести и распространенности кожного процесса. Автором разработан дизайн исследования, проанализированы результаты клинических и лабораторных методов обследования, проведен статистический анализ полученных данных. Разработаны практические рекомендации по применению комбинированного метода лечения микробной экземы.
Объем и структура диссертации.
Диссертация изложена па 137 страницах машинописного текста. Работа состоит из введения, обзора литературы, описания методов исследования, грех глав собственных наблюдений, заключения, выводов, практических рекомендаций. Список литературы содержит 278 наименований, из которых 174 — отечественных и 104 -иностранных авторов. Диссертация иллюстрирована 20 таблицами и 8 рисунками и графиками.
СОДЕРЖАНИЕ РАБОТЫ Клиническая характеристика больных, методы исследования и лечения.
Обследования больных проводились в соответствии с поставленными целями и задачами . В стационарных условиях клиники кожных и венерических болезней ГБОУ ВПО СамГМУ проведено обследование и лечение 114 больных микробной экземой, из них 49 (43%) мужчин, 65 (57%)женщин. Возраст больных варьировал от 15 до 76 лет. Микробная экзема чаще встречается в возрасте от 15 до 40 лет и старше 50 лет. В возрастных группах от 15 до 40 лет и старше 60 лет женщины болеют намного чаще, чем мужчины; в 41 — 50 лет — мужчины чаще. В возрасте 51-60 лет заболеваемость у мужчин и женщин одинаковая (таблица 1).
Пол/Возраст Число наблюдений Всего, %
15-20 4 9 13 (10,8%)
21-30 12 20 32 (28,3%)
31-40 6 10 16(14,2%)
41-50 9 4 13 (10,8%)
51-60 12 10 22 (20,0%)
Старше 60 6 12 18 (15,8%)
Итого 49 65 114(100%)
Тяжесть течения микробной экземы оценивали по шкале EASI(Eczema Area and Severity Index). Расчёт иидекса EASI основан на объективной оценке (интенсивности и распространённости кожных поражений). Каждый из четырёх объективных признаков (эритема, инфильтрация/папулы, экскориации и лихенизация) оценивался по 4-х уровневой шкале: 0 — отсутствие, 1 — слабые, 2 — умеренные, 3 — сильные.
Распространённость поражения кожи оценивалась по правилу «девятки», где за единицу принята площадь ладонной поверхности кисти. Индекс EASI рассчитывался по формуле: EASI = А + В + С + D, где А — общая сумма баллов (выраженность и распространённость кожного процесса) на коже лица, В — общая сумма баллов (выраженность и распространённость кожного процесса) на коже туловища, С -общая сумма баллов (выраженность и распространённость кожного процесса) на коже верхних конечностей и D — общая сумма баллов (выраженность и распространённость кожного процесса) на коже нижних конечностей.
Оценка интенсивности зуда производилась при помощи следующих параметров: 0 баллов — отсутствие зуда, 1 балл — слабый, 2 балла — незначительный, 3 балла — средней интенсивности, 4 балла — сильный.
Оценка эффективности терапии МЭ проводилась с использованием клинических критериев: выздоровление, значительное улучшение, улучшение, без эффекта. Под выздоровлением понимали полное разрешение очагов МЭ. Значительным улучшением считали стойкую положительную динамику процесса, характеризующуюся уменьшением EASI в 4 раза. Под улучшением — медленную, но положительную динамику с уменьшением EASI в 2 раза. Учитывалась трансформация непрерывного течения заболевания в рецидивирующее. Фиксировались переносимость лечения и медикаментозные осложнения.
Лечебным эффектом считалось полное исчезновение или уменьшение индекса EASI на 50% и больше.
Изучение микробного биоценоза кожи проводилось культуральным методом согласно приказу МЗ РФ №535/1998. Идентификация выделенных культур осуществлялась по классификации А.К.Акатова с соавт.. (1983). При этом также изучали микрофлору кожи в группе клинически здоровых людей (60 человек) в возрасте от 14 до 60 лет.
Количественную обсемененность материала микрофлорой устанавливали по числу колониеобразующих единиц (КОЕ) и определяли показатель микробной обсемененности кожи (КОЕ/чашка). Для изучения чувствительности к антибиотикам использовали метод диффузии в агар с применением стандартных бумажных дисков с
набором антибиотиков. Оценка степени чувствительности микробной флоры к антибиотикам проводилась по зонам задержки роста. Микробный штамм считался устойчивым к исследуемым антибиотикам, если зона задержки роста была менее 15 мм, чувствительным при зоне от 15 до 25 мм, высокочувствительным при зоне более 25 мм.
Иммунологические исследования выполнены в соответствии с рекомендациями ВОЗ и отечественных авторов (Петров Р.В. и соавт., 1992; Сидоренко Г.И. и соавт., 1992; Хаитов P.M., Пинегин Б.В., Истамов Х.И., 1995; Хаитов P.M., 2002) на базе иммунологического отдела ЦНИЛ ГБОУ ВПО СамГМУ Росздрава (директор — д.м.н., профессор Л.Т.Волова, зав. — к.б.н., доцент Л.В.Лимарева), иммунологической лаборатории кафедры общей и клинической микробиологии, иммунологии и аллергологии ГБОУ ВПО СамГМУ Росздрава (зав. кафедрой — д.м.н., профессор А.В.Жестков).В контрольную группу вошли 64 донора Самарской областной станции переливания крови, в возрасте 18-55 лет (48,2±2,1), 50 мужчин и 14 женщин. Все они не имели каких-либо хронических заболеваний уха, горла и носа, других органов и систем, по данным комплексного обследования были признаны здоровыми. Обследованные лица контрольной группы не имели признаков различных синдромов поражения иммунной системы.
Иммунологические методы исследования включали определение субпопуляций лимфоцитов с помощью моноклональных антител серии ИКО (МедБиоспектр, г. Москва). Вычисляли процент лимфоцитов крови, экспрессирующих CD3, CD4, CD8, CD 16, CD20, CD25, CD95, HLA-DR маркеры. Одновременно проводили клинический анализ крови для определения абсолютного количества клеток (Dahl R., 1993).
Содержание иммуноглобулинов А, М, G в сыворотке определяли методом Манчини (радиальная иммунодиффузия). Для оценки состояния нейтрофилов периферической крови использовали полистеральный латекс (ДиаМ, Россия); устанавливали процент клеток, фагоцитирующих частицы. Гемолитическую активность комплемента СН50 и миелопероксидазы определяли с помощью стандартных реакций. Концентрацию ИНФ-у (пг/мл) и интерлейкинов ИЛ-1а, ИЛ-lß, ИЛ-8, ФНО-а (пг/мл) в сыворотке крови исследовали с помощью твердофазного иммуноферментного анализа на многоканальном спектрофотометре «Dynatech MR 5000» (США) при длине оптической волны 492 нанометра.
Для обработки численного материала нами использовались современные методы многомерного статистического анализа с оценкой достоверности диагностической значимости каждого показателя иммунного гомеостаза: дескриптивная статистика, корреляционный, факторный, кластерный и дискриминантный анализ (Айвазян С.А., Мхитарян B.C., 1998; Гланц С., 1999; Боровиков В.П., 2001; A fifi A.A., Ansen S.P., 1984; Altman D.O., 1991).Обработка полученных данных проводилась в среде специализированного пакета «Excel» фирмы «Microsoft» и в системе «Statistica 6.0» фирмы «StatSoft» (США). Все величины переводились в значения, принятые в системе единиц СИ.
Согласно целям и задачам исследования все пациенты были распределены по полу, возрасту, степени тяжести процесса, клинической форме процесса, а затем разделены на 2 группы: 1-ая группа (основная), 58 человек, 2-ая группа (сравнения),
56 больных. В комплекс лечебных мероприятий входила гипоаллергенная диета с исключением облигатных и причинно-значимых аллергенов, ограничение контакта с возможными аллергенами в быту.
Все больные микробной экземой получали: дезинтоксикационнуга терапию, антигистаминные, гипосенсибилизирующие, седативные препараты. Местно — анилиновые красители
Для второй группы (сравнения)использовали комбинированное лекарственное средство, содержащее бетаметазона дипропионат 0,05%, гентамицина сульфат 0,1% и клотримазол 1%.
физиотерапевтическую установку Комбис-1, которая позволяет осуществить комбинированное воздействие низкоинтенсивным излучением лазера и распыленными жидкими лекарственными препаратами на очаги микробной экземы(разработано на кафедре госпитальной хирургии ГБОУ ВПО СамГМУ Росздрава совместно с кафедрой «Автоматических систем» Самарского государственного аэрокосмического университета (Б.Н. Жуков, В.Е. Костяев, A.B. Ревякин)).
Результаты собственных исследований и их обсуждение.
У наблюдавшихся больных были установлены различные формы микробной экземы в разных стадиях болезни. Среди наблюдавшихся нами больных типичная форма микробной экземы и варикозная выявлялась с частотой (55,3% — 63 больных и 28,9% -33 больных соответственно). Паратравматическая — у 18 больных (15,8%).У (51 человек — 44,7%)отмечено обострение хронической микробной экземы, у 47 (41,2%) -подострое течение. В анамнезе этим больным проводились различные варианты терапии, преимущественно антибиотикотерапия в сочетании с наружной терапией кортикостероидным препаратом. Ранее лечение не получали 16 пациентов (14,1%) с острым течением.
Длительность заболевания микробной экземой у обследованных больных колебалась от нескольких месяцев до 20 и более лет. Большинство больных — 84 (73,7%) — страдали микробной экземой больше 1 года, а 59 (51,8%) — свыше 5 лет.
Среди наблюдавшихся больных типичная микробная экзема в основном встречалась в возрасте от 15 до 40 лет, варикозная — у больных старше 50 лет, паратравматическая — преимущественно в возрастной группе 41-50 лет.
У большинства больных — 79 (69,3%) — обострения микробной экземы, происходили чаще в осенне-зимне-весеннее время года, у 35 (30,7%) — в любое .
У 67 (58,8%) больных патологический процесс на коже носил распространенный характер, у 47 (41,2%) — ограниченный. Следует отметить, что среди 63 больных с типичной формой микробной экземы распространенный процесс имели 49 (77,7%) пациентов, из 33 с варикозной -14(42,4%), из 18 с паратравматической — 4 (22,2%).
Очаги МЭ преобладали на кистях (39,2%), ягодицах и голенях (по 24,3%), на предплечьях (21,6%) и лице (18,9%). Реже локализовались на стопах (13,5%) и бедрах
(12,2%). Типичпа локализация на открытых участках кожного покрова (лицо, шея, кисти, стопы) была у_£77%) больных. Верхние конечности вовлекались в процесс чаще, чем нижние (73% против 56,8%).
Основным показателем оценки тяжести микробной экземы является индекс EAS1. Исходные значения индекса EASI у всех пациентов колебались в пределах от 4,5 до 26,7 и, в среднем, составили 18,6. Была установлена положительная корреляция зависимости возраста и течения экземы (г=0,3) у больных в возрасте старше 50 лет. Наиболее тяжёлое течение отмечалось у больных в возрасте от 5 1 до 60 лет — индекс EASI 25,12±0,26и в возрасте от 61 до 76 лег — индекс EASI — 32,49±2,16.
Сопутствующие заболевания были выявлены у 89 (78%) больных, причем 21 (18,3%) пациент имели сопутствующие аллергические заболевания.
Вредные привычки (употребление алкоголя, курение) имели 41 (35,9%) больной.
Обострения микробной экземы 18 (15,8%) больных связывали с обострением сопутствующих аллергических заболеваний, 23 (20,2%) — с обострением сопутствующих заболеваний неаллергического происхождения и простудными факторами, 15 (13,2%) — с нервно-психическими потрясениями, 23 (20,2%) — с употреблением в пищу различных продуктов, обладающих аллергенными гистаминолиберагорными свойствами (яичные блюда, соленья, кофе и шоколад, бобовые, перец, уксус, цитрусовые, алкоголь и др.) и лекарственных препаратов, 35 (30,7%) — с профессиональными вредностями и использованием различных моющих средств.
Наследственную предрасположенность к аллергическим заболеваниям имели 28 (24,6%) больных.
Изучение структуры микрофлоры очагов поражения проводили у 114 больных микробной экземой. При этом также изучали микрофлору кожи в группе клинически здоровых людей (60 человек) в возрасте от 14 до 60 лет.
Основной характеристикой микробиоценоза кожи при микробной экземе являлось следующее: частота высева стафилококков на пораженном участке составила 89,7±6,4%, частота высева Staphylococcus aureus — 64,9±5,1%, St.epidermidis -43,3±2,4%, St.saprofitis — 3,3±0,9%. Процент высева стрептококков — 15,4±1,9%, Streptococcus pyogenes — 5,0±1,3%. Грамположительные бактерии обнаруживались (6,3±0,7%) в основном за счет Corinebacterium и Propionebacterium. Частота обнаружения грамотрицательных бактерий — 16,6±1,5%, за счет бактерий рода Proteus, Klebsiella и E.coli. Зарегистрировали увеличение частоты выделения в зоне воспаления условно-патогенной флоры — 2,8±0,4%.
Характер микробиоценоза кожи обусловлен ассоциациями Staphylococcus aureus, Streptococcus pyogenes и грамотрицательных бактерий. У 75 (65,8%) больных микроорганизмы высеивались в виде ассоциации 2-3 микроорганизмов. Стафилококки монокультурой выделялись в 21,0% случаев (St.aureus — у 19% больных), стрептококки — в 6,7%, причем у всех больных высеян Str.pyogenes.
Второй характеристикой микробиоценоза кожи при микробной экземе является плотность высева микроорганизмов: стафилококки — 48,4±4,3 КОЕ/чашка. Плотность высева стрептококков повышена — 24,9±2,3 КОЕ/чашка, грамположительных бактерий
немного снижена — 12,9±1,5 КОЕ/чашка, грамотрицательных бактерий повышена -35,7±3,б КОЕ/чашка и условно-патогенной флоры — 4.5±0,5 КОЕ/чашка. У 27 (23,7%) больных отмечен очень высокий уровень обсемененности (сплошной рост колоний).
В очагах поражения при микробной экземе отмечается значительный рост грамположительной кокковой флору. представленной r основном Staphylococcus, в меньших количествах — Streptococcus, при высокой обсемененности микроорганизмов. Плотность грамотрицательных бактерий в зоне поражения также значительно возрастали. Численность других грампозитивных бактерий несколько снижалась, но без достоверных различий. Численность условно-патогенных возбудителей и грамотрицательных палочек значительно возрастала
Таким образом, патогенные микроорганизмы S.aureus и S.pyogenes вытесняют представителей резидентной микрофлоры (S.epidermidis, Corynebacterium sp..), что свидетельствует об участии патогенной флоры в кожном процессе.
Учитывая это, определение чувствительности возбудителей к широкому набору современных антибактериальных средств имеет первостепенное значение при выборе наиболее эффективного препарата. Поэтому следующим этапом исследования явилось изучение антибиотикочувствительности. Высокая чувствительность была отмечена в 7% случаев к ципрофлоксацину, цефазолину, цефобиду, цефтриаксону и рулиду. Средняя чувствительность определялась в 29% к офлоксацину, доксициклину, эритромицину. Минимальная чувствительность ко всем используемым антибиотикам отмечена в 64% случаев.
Следующим этапом исследований стал анализ диагностического, прогностического и дифференциально-диагностического значения методов оценки клеточных и гуморальных факторов иммунитета, а также цитокинового статуса. Дескриптивная статистика показателей, характеризующих клеточные факторы иммунитета, представлена в таблице № 2.
Дескриптивная статистика показателей, характеризующих клеточные факторы иммунитета
Показатели Больные МЭ (х» ± s) (n=l 14) Контрольная группа (х» ± s) (п=64) 2,14 ± 0,06
Лимфоциты абс. 2,78± 0,14
СПЗ+ клетки 410′, абс. 2,03 ±0,10 1.49 ± 0.04
СОЗ+ клетки, %. 72,75 ±0.52 71.37 ± 0,52
СР4+ клетки х|0’\ абс. 1,30±0,06 1,32 ± 0.04
СР4+ клетки, %. 47,63± 0,58 45,08 ±0,38
СП8+ клетки ИО’, абс. 0,65± 0,04 0,60 ± 0,03
СЭ8+ клетки, %. 21,98± 0,41 * 25.98 ± 0,33
С04+/С08+ 2,30± 0,06* 1,75 ± 0,03
СО 16+ клетки хюу, абс. 0,36± 0,02 0,22 ±0,01
СО 16+ клетки, %. 12,33± 0,53* 17,86 ± 0,23
С020+ клетки *10ч, абс. 0,33± 0,02 0,34 ±0,01
С020+ клетки, %. 11,87± 0,51 15,89 ±0,33
С025+ клетки *10″, абс. 0,67± 0,03* 0,13 ±0,02
С025+ клетки, %. 25,91 ± 1,11** 3,91 ± 0,12.
С095+ клетки, %. 23,91± 0,89** 10,22 ± 0,28
НЬА-ОЯ+клегки * 10ч, абс. 0,72 ±0,04** 0,18 ±0,002
НЬЛ-ОЯ+клетки, %. 26,26 ±0,81** 10,46 ± 0,23
ФАЛ, % 48,30± 0,72* 59,35 ± 1,01
Миелоиероксидаза, % 58,67 ± 0,30** 46,29 ± 0,39
Анализ показателей клеточных факторов иммунитета у обследованных пациент показал, что в группе больных МЭ, отмечается повышение уровней: общего количества лимфоцитов, клеток экспрессирующих на своей поверхности НЬА-ОЯ+, СЭЗ+, СЭ4+, С025+, СЭ95+ маркеры, индекса СЭ4+/С08+ и снижение содержания клеток, экспрессирующих СЭ8+, СО 16+ маркеры и фагоцитарной активности лейкоцитов.
Различия между группами обследованных пациентов достоверны с высокой степенью значимости по следующим показателям: количество клеток, экспрессирующих на своей поверхности СЭ8+, С016+(р<0,05), Н1_А-011+, С025+, С095+ (р<0,01), иммунорегуляторный индекс и ФАЛ (р<0,05). Достоверность различий между группами нами оценивалась с помощью дисперсионного анализа.
Изменения в клеточном звене выражаются в его угнетении, о чем свидетельствует низкий по сравнению с данными здоровых доноров уровень клеток экспрессирующих С08+ маркеры, что приводит к повышению иммунорегуляторного коэффициента. Повышенный коэффициент С04+/С08+ у больных МЭ, указывает на остроту процесса. Кроме того увеличение иммунорегуляторного индекса в исследуемой группе сопутствует аллергическим реакциям.
Снижение клеток экспрессирующих С08+ и С016+ маркеры, возможно, связано с их перераспределением в очаг воспаления в коже, что сопровождается их гибелью и понижением уровня в крови. Низкая концентрация клеток экспрессирующих СЭ8+ и СЭ16+ маркеры компенсируется общим увеличением содержания лимфоцитов.
Тенденция к более высокому содержанию клеток экспрессирующих С04+ маркеры никак не определяет лучший антибактериальный иммунный ответ, о чем
свидетельствует выраженная клиническая картина. По-видимому, отсутствие защитного потенциала, связано с тем, что в ходе иммунного ответа на инфекционный агент необходима последовательная активность включения различных популяций Т-хелперов.
Повышенный уровень готовности клеток к апоптозу (запрограммированная гибель клеток) — увеличение количества клеток экспрессирующих С095+ маркеры -может указывать на снижение относительного количества клеток экспрессирующих на своей поверхности СЮ8+, СО 16+ и С020+ маркеры за счёт этого механизма. Выявлена активация процесса апоптоза в исследуемой группе, так как значение СЭ95+ у больных МЭ повышено.
Отмечено увеличение количества антигенпрезентирующих лимфоцитов экспрессирующих маркер активации Т-лимфоцитов НЬА-ЭК+, что может являться свидетельством» адекватной реакции иммунной системы на антигенный стимул. Иммунная реакция на экзему, как любой воспалительный процесс, формируется посредством ли’мфопролиферации и активации Т-клеток преимущественно через НЬЛ-
Известно, что активность фагоцитов во многом определяется участием главного комплекса гисто’совместимости. Поэтому при микробной экземе наиболее резко снижена активность фагоцитов. Одними из первых в неспецифической защите организма от инфекции проявляются фагоцитарные реакции, отвечая практически сразу на внедрение инфекционного агента. При этом фагоцитарные клетки не только препятствуют распространению чужеродных агентов в тканях человека, но и уничтожают их, параллельно стимулируя деятельность Т — звена иммунитета. У больных микробной экземой определено выраженное подавление фагоцитарной активности лейкоцитов по сравнению со здоровыми, что свидетельствует о снижении поглотительной способности нейтрофилов. Подавление ФЛЛ, возможно, является следствием ингибирующего влияния токсинов и ферментов патогенных и условно-патогенных микроорганизмов, в первую очередь 51.аигеия и 81.ер1с1егггпсП5 на ферментный и рецепторный аппарат нейтрофилов. Выявленные при экземе нарушения процессов фагоцитоза способствуют персистенции инфекции в коже, развитию сенсибилизации и аутосенсибилизации. Кроме того, регистрируется повышение активности миелопероксидазы (р<0,01).
Регистрируется увеличение содержания клеток, активированных посредством интерлейкина-2 (СД25+) у больных микробной экземой.
Необходимо отметить, что при микробной экземе имеются значительные нарушения иммунного статуса у больных, выражающиеся в качественной и количественной недостаточности клеточного звена иммунитета и дисбалансов показателей иммунной системы. Указанные изменения играют важную роль в возникновении и дальнейшем развитии заболевания.
Следующим этапом было определение показателей, характеризующих гуморальные факторы иммунитета у больных МЭ (таблица № 3).
Дескриптивная статистика показателей, характеризующих гуморальные факторы иммунитета
Показатели Больные МЭ (х- ± ¡)(п=114) Контрольная группа (х
^А, г/л 2,57± 0,06* 1,82 ±0,02
г/л 12,86± 0,34* 14,53 ±0,27
1цМ, г/л 1,09± 0.03 1,14 ± 0,02 .
Активность комплемента, е.а. 46,18± 0,19** 50,05 ± 0,17
ЦИК 2,30± 0,06* 1,75 ±0,03
Анализ показателей дескриптивной статистики у лиц обследованных групп выявил следующие особенности иммунологического реагирования показателей гуморальных факторов. В исследуемой группе отмечается изменение гуморального иммунного ответа (повышение сывороточных концентраций ^А и снижение ^М, активности комплемента).
Различия между группами обследованных пациентов достоверны с высокой степенью значимости по следующим показателям: комплементарная активность сыворотки крови больных (р<0,01) и уровень ^А (р<0,05). Достоверность различий между группами нами оценивалась с помощью дисперсионного анализа.
Несостоятельность рецепторного аппарата фагоцитирующих клеток является одной из причин повышения циркулирующих иммунных комплексов.
Нарушения в системе Т-клеточного иммунитета приводят к изменению взаимодействия с клоном В-лимфоцитов, начинающих продуцировать в избыточном количестве иммуноглобулин А. Отмечается снижение уровня С020+лимфоцитов. Такие изменения приводят к более тяжелым поражениям организма антигеном.
Низкий уровень ^М у больных с МЭ, свидетельствует об отсутствии присоединения новых возбудителей, так как 1§М вырабатывается при первичном контакте с антигеном. Кроме того, уменьшение содержания В-клеток и низкая концентрация обусловлены длительной микробной сенсибилизацией организма.
Образование и отложение ЦИК в тканях гак же связано с дефицитом Т-системы и её субпопуляций.
Был проведен корреляционный анализ между уровнями иммуноглобулинов ^А, ^М, ^О и СЭ20+, НЬА-ОК+ клетками. Сопоставление колебаний уровней
гуморальных . факторов и СЭ20+, НЬА-ОК+ клеток выявило статистически достоверную зависимость между значениями СР20+ и НЬА-011+
Было проанализировано участие провоспалительных цитокинов и ИНФ-у в иммунопатогенезе МЭ. Мы определяли уровни ИЛ-1а, ИЛ-10, ИЛ-8, ФНО-а и ИНФ-ув сыворотке крови (таблица № 4).
Дескриптивная статистика показателен, характеризующих цитокиновый статус
Показатели Больные МЭ (х
± э) (п=114) Контрольная группа (Г + (п=64)
Ил-1а, пг/мл 11,91+0,25*** 0
Ил-10, пг/мл 5,54+ 0,20*** 30,72 + 0,29
Ил-8, пг/мл 62,67+ 0,66*** 15,78 + 0,51
ФНО-а, пг/мл 22,79+ 0,35*** 46,02 + 0,55
ИНФ-у, пг/мл 119,82 ± 0,44*** 191,54+ 1,49
Различия изучаемых показателей между группами обследованных пациентов достоверны с высокой степенью значимости. Достоверность различий между группами по показателям ИЛ-8, ИЛ-1а, ИЛ-10, ФНО-а и ИНФ-у нами оценивалась с помощью дисперсионного анализа.
При анализе функциональной активности Т-лимфоцитов отмечается повышение уровня НЬА-ОК+, что косвенно указывает на повышенную продукцию цитокинов.
Концентрация ИЛ-8, ИЛ-1а увеличена, так как идет активный воспалительный процесс в коже. Высокий уровень ИЛ-1а активирует Т-клеточный ответ на антигены, а соответственно способствует увеличению маркера активации Т-лимфоцитов НЬА-011+. Кроме того стимулирует синтез иммуноглобулина А и ИЛ-8.
Отсутствие высоких значений уровня ФНО-а в исследуемой группе, по-видимому, обусловлено снижением количества клеток экспрессирующих СО 16+ маркеры, которые также выделяют ФНО-а под действием ИЛ-1.
Снижение ИНФ-у косвенно свидетельствует об угнетении специфического клеточного иммунного ответа.
Учитывая возможное сочетание изменений клеточных, гуморальных факторов и активацию цитокинов в ходе иммунного ответа нами были проанализированы
закономерности формирования типов иммунных реакций у больных микробной экземой.
Для более точной математической оценки полученных результатов исследования клеточных и гуморальных факторов иммунитета, а также цитокинового статуса нами проведен факторный анализ (метод главных осей).
Оптимальное решение было найдено в размерности 3. Мы.; полагаем, что факторная структура изучаемой выборки является отражением реакций организма при развитии микробной экземы у больных. Проведенный анализ выделенных факторов показывает, что фактор 1 определяется абсолютным содержанием лимфоцитов и клеток, экспрессирующих СЭЗ+, С04+, СЭ8+, СЭ20+,. СЭ95+ и НЬА-маркеры; фактор 2 характеризуется уровнем клеток, экспрессирующих СЭ16+ маркеры, ФАЛ и ФНО-а, он описывает элиминационные механизмы в процессе иммунного ответа; фактор 3 определяется уровнем клеток, экспрессирующих С020+ маркеры и ИЛ-8, ИЛ-1Р. Суммарно эти три фактора объясняют 59,4% дисперсии анализируемой статистической выборки.
С учетом результатов факторного анализа проведен кластерный анализ методом к-средних по выявлению различных типов иммунного гомеостаза. Группирующие переменные формировались с применением дисперсионного анализа. В модель включались только те показатели, значимый р-уровень которых не превышал 0,05 (рисунок 1).
Рис. 1. Результаты кластерного анализа показателей типа иммунного ответа при микробной экземе
Обследуемые по типу реагирования иммунной системы четко разделились на два кластера. Первый кластер (тип реагирования иммунной системы при экземе) характеризовался более высокими уровнями исследуемых показателей иммунитета (лимфоциты, клетки, экспрессирующие СОЗ+, СЭ8+, СБ95+ и НЬА-01<+ маркеры).
Второй тип реагирования гомеосгаза у больных экземой, характеризовался достоверно высоким уровнем исследуемых показателей иммунитета (клетки экспрессирующие С04+, СБ 16+ и СБ25+ маркеры).
Для проверки значимости основного фактора (тип реагирования иммунной системы) в полученной модели был проведен многомерный дисперсионный анализ всех исследуемых показателей. Суммарный анализ дискриминантных функций, на основании которых строилась дискриминантная модель типов иммунного реагирования, показал, что полученная модель достоверно характеризует анализируемую выборку (Х-критерий Уилкса = 0,29; Р(3,84)=27,32, что дает значимый результат р<0,00001). В результате проведенных нами кластерного и дискриминантного анализов, можно признать адекватной полученную классификацию типов иммунных реакций организма.
Таким образом, выделено два типа реагирования иммунной системы у больных МЭ. При этом с помощью дискриминантных функций можно вычислить классификационные метки типов иммунного ответа организма по следующим формулам:
Тип I. (формула 1):
ИКТРО, = 9,51л + 1,З СЭЗ- 21,8034 — 1,З СЭ8 + 3,70)16 + 19,7С095 н 1,6НЬА-ОК + 2,2С025 — 9,4, где ИКТИС, — интегральный коэффициент реакцш организма первого типа;
Тип 2. (формула 2):
ИКТР02 = — 12,11л — 1,7-СОЗ + 27,9-СЭ4 + 1,6 С08 — 4.8 С016 — 25,2Ш95 2,1 НЬЛ-ВЯ — 2,8 С025 — 15,0, где ИКТИС2 — интегральный коэффициент реакции организма второго типа. V
Обследуемый пациент будет относиться к тому типу, для которого значение ИКТРО (интегрального коэффициента реакции организма) будет максимальным. Первый тип иммунных реакций, отмеченный у 64 пациентов,: сопровождала распространенностью кожного процесса. Второй тип иммунных реакций взаимосвязан с локализованными формами микробной экземы, он был определен у 50 больных МЭ.
Таким образом, разработанная дискриминантная модель позволяет использовать на практике полученную классификацию типов иммунных реакций организма ; пациентов с МЭ. Определяя указанные параметры клеточных факторов иммунитета, мы можем прогнозировать течение микробной экземы и угрозу развития распространенного процесса. В изученной нами литературе не обнаружено данных о типах иммунного реагирования при микробной экземе.
Результаты комбинированного лечения больных микробной экземой.
Курс лечения состоял из 10-15 процедур установкой Комбис-1, проводимых ежедневно с учетом индивидуальных особенностей каждого больного и микрофлоры. Дозы лазерного воздействия соответствовали «Санитарным нормам и правилам устройства и эксплуатации лазеров» (1985). Препараты, используемые для орошения поверхности МЭ, применяли в соответствии со стадией процесса, чувствительности микрофлоры к антибактериальным средствам. Наиболее часто используемыми препаратами для орошения были следующие антибактериальные средства: ципрофлоксацин, цефазолин, цефобид, цефтриаксон, рулид, офлоксацин, доксициклин 1 эритромицину, в сочетании с раствором дексаметазона. Скорость распыления препаратов составляла 0,2-0,5 мл/мин, длина волны лазерного излучения 0,63 мкм; плавная регулировка плотности мощности лазерного излучения в зоне патологического очага — 0,5 — 15 мВт/см2; диапазон регулировки диаметра светового пятна на обрабатываемой поверхности — 10-100 мм; давление сжатого воздуха для распыла жидкого лекарственного препарата — 0,5-1,5кгс/см, экспозиция 5-8 минут. 3 процедуру облучалось до 5 полей при общей продолжительности не более 30 минут.
Критерием оценки терапевтической эффективности, предложенного комбинированного лечения микробной экземы, считали прекращение зуда, частичное или полное разрешение эритемы, уменьшение отека и инфильтрации, эпителизацию эрозий, рубцевание трофических язв на фоне хронической венозной недостаточности нижних конечностей или травматических повреждений кожи, значительное улучшение общего самочувствия (непосредственные результаты). Всем пациентам в группе для
оценки результатов лечения перед началом исследования, через месяц и 6 месяцев производили оценку индекса EASI.
Переносимость комбинированной терапии в этой группе больных была хорошей. У 2 больных в течение трёх дней было трапзиторное ощущение жжения после проведения процедуры, которое не потребовало отмены процедур. Дальнейшее использование предложенного метода лечения не привело к побочным эффектам.
Динамика: зуд, как основной субъективный признак микробной экземы, начал ослабевать в среднем с 3-4 дня лечения, у большинства больных полностью прекратился в среднем к 8-9 дню, у всех больных — к 12-13 дню. Побледнение эритемы и уменьшение отека началось в среднем с 3-4 дня, их исчезновение произошло в среднем к 15-16 дню. Инфильтрация кожи в очагах поражения начала уменьшаться в среднем с 6-7 дня, полностью разрешилась — к 11-12 дню. Отторжение корок и чешуек происходило с 4-5 дня терапии, завершившись в среднем к 7-8 дню.
У больных варикозной и паратравматической экземой отмечена четкая положительная динамика со стороны признаков патологии кровообращения и нарушения трофики тканей. Так, к 7-8 дню терапии полностью исчезали судороги мышц голеней, боли в области голеней, чувство «онемения», «перетяжки» в нижней 1/3 голени. К концу курса лечения значительно снижалась утомляемость в конечностях при ходьбе, зябкость кистей и стоп. Рубцевание трофических и раневых язв произошло в среднем в 17-18 день. Следует отметить, что даже пожилые пациенты отмечали заметное улучшение общего самочувствия, ощущение «легкости» при ходьбе.
Клиническое выздоровление — полное разрешение клинических признаков экземы (исчезновение зуда, эритемы, отека, инфильтрации, отторжение корок) к концу комбинированного курса лечения зарегистрировано у 35 (60%) больных. Значительное улучшение (исчезновение эритемы, отека, инфильтрации, слабый зуд) было достигнуто у 18 (32%) пациентов. Улучшение (незначительная эритема в некоторых бывших очагах, умеренная инфильтрация, слабый зуд) наступило у 5 (8%) больных.
В первой группе больных микробной экземой, регистрировалась ярко выраженная положительная динамика средних значений индекса EASI.
Согласно расчётам, средние значения индекса EASI в этой группе больных в результате лечения снизились с 18,34±1,71 до 0,8±0,11 (95%) и через полгода после окончания терапии индекс EAS1 в этой группе равнялся, в среднем, 3,4±2,3 (13%) (р<0,05). Выраженная положительная динамика результатов объективной оценки состояния кожных покровов после проводимой терапии у больных микробной экземой свидетельствует о наибольшей эффективности комбинированной терапии.
Таким образом, удовлетворительные результаты лечения отмечены у больных, имевших выраженную поливалентную сенсибилизацию, с длительностью заболевания свыше 10 лет, с частыми обострениями экзематозного процесса и неоднократно лечившиеся во время обострений дерматоза антибактериальными и кортикостероидными препаратами.
Средняя продолжительность пребывания в стационаре больных микробной экземой, получивших комбинированное лечение, составила 14,7±1,4 койко-дней.
Оценка результатов лечения проводилась и по данным лабораторных исследований.
Применен метод бактериологического контроля состояния очагов. Исследовани! выполнялись в середине курса (на 10-12 день) и по окончании лечения (20-22 день (таблица 5).
Микрофлора кожи больных МЭ До лечения (n=l 14) Лечение (10-12 1 Лечение (20-22 день) (n=58) 1 день) (п=58)
St. aureus (%) 65 30.8 9,8*
St. epidermidis (%) 43,3 45,6 48,2
Str. pyogenes (%) 13,4 7,8 3,1*
Corinebacterium (%) 3,3 11,4 16,2
Роста нет (%) — 21 65*
При определении чувствительности к антибактериальным препаратам, в конце лечения высокая чувствительность наблюдалась в 33 (57%) случаев, а показатель устойчивости снизился до 7% (Р<0,01).
Результаты лечения больных микробной экземой в группе сравнения.
Все больные лечение перенесли хорошо, побочных явлений и осложнений не было. Зуд разной интенсивности, беспокоивший больных, начал уменьшаться в среднем с 5-6 дня терапии и у большинства больных полностью прекратился в среднем к 16-17 дню. Уменьшение отека кожи в очагах поражения и побледнение эритемы начались в среднем с 5-6 дня лечения, полное разрешение эритемы в очагах поражения у большинства больных произошло в среднем к 22-23 дню. Инфильтрация кожи в очагах поражения начала уменьшаться в среднем с 8-9 дня, полностью прошла 1 16-17 дню. Отторжение корок и чешуек в среднем началось с 5-6 дня, завершилось к 1011. У больных варикозной и паратравматической экземой положительная динамик; началась с 5-6 дня, чувство «онемения» в области голеней, судороги мышц исчезли полностью к 12-13 дню. Утомляемость в конечностях при ходьбе к концу курса лечения значительно уменьшилась. Рубцевание трофических язв началось в среднем с 7-8 дня терапии, полное их рубцевание произошло к 25-26 дню.
01 группа Ш2 группа
Во второй группе больных, где проводилась стандартная терапия больных микробной экземой, наблюдались следующие изменения тяжести клинической картины в соответствии с регистрацией индекса ЕА81.
Клиническое выздоровление к концу лечения отмечено у 13 (23,3%) больных, значительное улучшение — у 17 (30%), улучшение — у 17 (30%). Эффекта от проводимой терапии не было у 9 (16,7%) больных: 5 больных с типичной формой микробной экземы, 4-о варикозной.
Средняя продолжительность пребывания больных в стационаре составила 22,7±1,6 койко-дней.
Непосредственные результаты эффективности использованных методов лечения больных микробной экземой представлены в таблице 6.
Непосредственные результаты лечения больных микробной экземой по группам
Результаты Группы больных
I (основная) п=58 II (сравнения) п=56
Клиническое выздоровление 35 60 13 23,3
Значительное улучшение 18 32 17 30
Улучшение . 5 8 17 30
Без эффекта 0 0 9 16,7
Всего 58 100 56 100
Как видно из таблицы, наиболее эффективными при лечении больных микробной экземой был комбинированный методы с использованием традиционных средств и аппарата Комбис-1. При лечении аппаратом Комбис-1 в комплексе с обычными средствами положительный терапевтический эффект получен у 100% больных, из них у 92% клиническое выздоровление и значительное улучшение. Лечение только традиционными средствами привело к клиническому выздоровлению и значительному улучшению лишь у 53,3% больных и оказалось малоэффективным у 16,7% больных.
Под влиянием комбинированного метода лечения значительно уменьшились сроки пребывания больных в стационаре. Комплексное лечение с использованием аппарата Комбис-1 по сравнению с обычными средствами сократило сроки лечения больных в среднем на 7,9 дня (Р<0,001).
На фоне лечения показатели микробной обсемененности и биологические свойства возбудителей могут изменяться. В связи с этим динамическое обследование микрофлоры кожи может служить прогностическим тестом эффективности лечения. Применен метод бактериологического контроля состояния очагов. Исследования выполнялись в середине курса (на 10-12 день) и по окончании лечения (20-22 день) (таблица 7).
Микрофлора кожи больных До лечения Лечение (10-12 Лечение (20-22
сМЭ (n=l 14) день) (п=56) день) (п=56)
St. aureus (%) 65 40,8 29,8
St. epidermidis (%) 43,3 43,6 43,2
Str. pyogenes (%) 13,4 10,8 7,1
Corinebacterium (%) 3,3 5,4 6,2
E. coli (%) 5 3,8 3,1
При определении чувствительности к антибактериальным препаратам, в конце лечения высокая чувствительность наблюдалась в 16 (29%) случаев, а показатель устойчивости снизился до 21 (38%).
Таким образом, исследованиями установлена недостаточная эффективность традиционных методик в отношении их влияния на бактериологический фон, что проявляется толерантностью микробной флоры к использованным антибиотикам широкого спектра действия.
В результате проведенных исследований получены данные о положительном действии комплексного лечения с использованием лазерного излучения па бактериологический статус у больных с микробной экземой. При сравнении аналогичных показателей установлено более выраженное бактериостатическое и бактерицидное действие.
Таким образом, у больных, которым были применены методы лазеротерапии при помощи физиотерапевтической установки, отмечены существенные положительные сдвиги в бактериологическом статусе. Подобных изменений у больных, которым применялась традиционная терапия, не было выявлено.
Непосредственные результаты лечения показали значительное преимущество комплексного метода лечения с использованием лазерного аппарата Комбис-1 по сравнению с традиционным лечением. Так, клиническое выздоровление к концу комбинированного курса лечения было отмечено у 35 (60%) из 58 наблюдавшихся больных основной группы, значительное улучшение — у 18 (32%), улучшение — у 5 (8%), т.е. положительная клиническая динамика наблюдалась у всех больных. В группе больных, получавших традиционное лечение, клиническое выздоровление было достигнуто только у 13 (23,3%) пациентов, значительное улучшение — у 17 (30%), улучшение также у 17 (30%), а эффекта от терапии обычными средствами не отмечено у 9 (16,7%) больных. Т.е. предложенный нами комбинированный метод лечения больных микробной экземой с использованием аппарата Комбис-1 оказался эффективнее.
Отбор для обследования проводился методом случайной выборки, отвечающей требованиям репрезентативности по отношению к генерализованной совокупности.
Выполнено клиническое обоснование комбинированного метода воздействия на очаг микробной экземы низкоинтенсивным лазерным излучением и лекарственным препаратом, подаваемым в патологический очаг в мелкодисперсном состоянии.
1. Данные клинических и бактериологических исследований у больных с микробной экземой позволяют прогнозировать течение заболевания и развитие распространенного процесса.
2. Развитие микробной экземы обусловлено в 66,7% случаев ассоциациями стрептококка со стафилококком или с грамотрицательной флорой.
3. У пациентов с микробной экземой отмечается достоверное повышение уровня клеток, экспрессирующих С025+,С095+ и НЬА-ОЯ+ маркеры, индекса С04+/’С08+, сывороточных концентраций ^А, ИЛ-8, ИЛ-1а и снижение уровня клеток, экспрессирующих СЭ8+ и СО 16+ маркеры, а также фагоцитарной активности
лейкоцитов, активности комплемента, сывороточных концентраций ИЛ-1(3, ФНО-а I ИНФ-у.
4. Больные с микробной экземой имеют два типа иммунного ответа по наиболе! значимым показателям, включенным в разработанную математическую модел! (лимфоциты, клетки, экспрессирующие СОЗ+, С04+, СЭ8+, СО 16+, С025+, С095+ I НЬА-ОИ+ маркеры). Первый тип иммунного ответа сопровождало! распространенностью кожного процесса. Второй тип иммунных реакций взаимосвяза! с локализованными формами микробной экземы.
5. Комплексный метод лечения больных микробной экземой с иcпoльзoвaниe^ аппарата Комбис-1 значительно эффективнее традиционного лечения: клинически выздоровление и значительное улучшение достигнуто соответственно у 92% и 53,3°/ больных; сократил сроки лечения больных в 1,6раза.
1. При проведении диагностики и прогнозировании развития микробноГ экземы рекомендуется дополнительный комплекс высокоинформативны: иммунологических тестов: иммунофенотипирование лимфоцитов крови, определен™ уровней провоспалительных цитокинов в сыворотке крови.
2. Для оценки индивидуальных реакций организма при микробной экземе предлагается использование разработанной нами математической модели.
3. С целью повышения эффективности лечения рекомендуется использование ; больных микробной экземой аппарата Комбис-1.
4. При амбулаторном наблюдении пациентов с микробной экземой целесообразно участие аллерголога-иммунолога с оценкой значимых показателе:» иммунного, цитокинового статуса и коррекцией лечебной программы с применением иммунотропных препарата.
Список работ, опубликованных по теме диссертации.
1. Никонова И.В. Иммунологические особенности развития микробной экземы. /Никонова И.В., Орлов Е.В., Лимарева Л.В., Коннов П.Е.// Материалы научно-практической конференции «Актуальные проблемы дерматовенерологии» посвященной 85-летию Самарской дерматовенерологии — Самара, 2009 — с.63-64.
2. Никонова И.В. Клинико-иммунологические особенности микробной экземы /Никонова И.В., Коннов П.Е., Лимарева Л.В.// Материалы 3 всероссийского конгресса дерматовенерологов — Казань, 2009 — с.43
3. Никонова И.В. Микробиологический пейзаж у больных с микробной экземой в Самарской области / Никонова И.В., Орлов Е.В., Концов П.Е.// Материалы IV междисциплинарной научно-практической конференции «Современные методы диагностики, лечения кожных болезней и инфекций, передаваемых половым путем» — Казань, 2011 — с. 218-221.
4. Никонова И.В. Состояние биоценоза кожи при микробной экземе /Никонова И.В., Орлов Е.В., Концов П.Е.// Практическая медицина», Казань — №2(49) — 2011 — с.80-83
5. Ннконова И.В. Клннико-микробиологнческне особенности микробной экземы и совершенствование методов лечения. / Никонова И.В., Орлов Е.В., Коннов П.Е.// Аспирантский вестник, «Медицина» 5-6 — 2011 — с.86-91
Подписало к печати 1!). 12.21)12. Фирчат (¡0x90/16 Бума! а офсетнам, Гариигура Times New Ruinan. Печать цифринаи. Усл.иечл. 1,37. Тираж 1Ш11KJ. Заказ Л« 864.
Отпечатано в тиипграфии Green cat ИГ] Сс/иш некий Н.С. г. Самара, ул. Миш 27-1У гел.ХУ272117195Г.
